книжки малышки ассоциации

Модель:
RUR 384
КРОШКА Я Набор маникюрный детский «Для Малышки», 4 предмета: ножнички, книпсер, пилочка, щётка Наборы инструментов для маникюра и педикюра

Модель:
RUR 599
HAIRDORABLES Малышки-сестрички «Мармеладная фантазия» 1.0 Игрушки

Модель:
RUR 245
FLEXPOCKET Сменный блок с листами в клетку для записной книжки Flexpocket Блокноты и записные книжки

Модель:
RUR 1286
Показания Сахарный диабет 2 типа для улучшения гликемического контроля при неэффективности диетотерапии и физических нагрузок: у взрослых в качестве монотерапии, в сочетании с другими пероральными гипогликемическими средствами или с инсулином. Противопоказания Противопоказания - повышенная чувствительность к алоглиптину или к любому вспомогательному веществу, или серьезные реакции гиперчувствительности к любому ДПП-4 ингибитору в анамнезе, в том числе анафилактические реакции, анафилактический шок и ангионевротический отек: - сахарный диабет 1 типа: - диабетический кетоацидоз: - хроническая сердечная недостаточность (функциональный класс III-IV по функциональной классификации хронической сердечной недостаточности Нью-Йоркской кардиологической ассоциации): - тяжелая печеночная недостаточность (более 9 баллов по шкале Чайлд-Пью) из-за отсутствия клинических данных о применении: - тяжелая почечная недостаточность: - беременность, период грудного вскармливания - в связи с отсутствием клинических данных по применению: - детский возраст до 18 лет - в связи с отсутствием клинических данных по применению. С осторожностью: Острый панкреатит в анамнезе (см. Особые указания). У пациентов с почечной недостаточностью средней степени тяжести (см. Особые указания). В комбинации с производным сульфонилмочевины или инсулином (см. Особые указания). Прием трехкомпонентной комбинации препарата Випидия с метформином и тиазолидиндионом (см. Особые указания). Беременность Не проводилось исследований применения алоглиптина у беременных женщин. Исследования на животных не показали прямого или непрямого негативного воздействия алоглиптина на репродуктивную систему. Однако в целях предосторожности применение препарата Випидия во время беременности противопоказано. Отсутствуют данные о проникновении алоглиптина в грудное молоко у людей. Исследования на животных показали, что алоглиптин проникает в грудное молоко, поэтому нельзя исключить риск возникновения побочных эффектов у грудных детей. В связи с этим применение препарата в период грудного вскармливания противопоказано. Применение и дозы Препарат принимают внутрь. Рекомендуемая доза препарата Випидия составляет 25 мг один раз в сутки в качестве монотерапии или в дополнение к метформину, тиазолидиндиону, производным сульфонилмочевины или инсулину, или в качестве трехкомпонентной комбинации с метформином, тиазолидиндионом или инсулином. Препарат Випидия может приниматься независимо от приема пищи. Таблетки следует проглатывать целиком, не разжевывая, запивая водой. В случае если пациент пропустил прием препарата Випидия, он должен принять пропущенную дозу как можно быстрее. Недопустим прием двойной дозы препарата Випидия в один и тот же день. При назначении препарата Випидия в дополнение к метформину или тиазолидиндиону дозу последних препаратов следует оставить без изменения. При комбинировании препарата Випидия с производным сульфонилмочевины или инсулином дозу последних целесообразно уменьшить для снижения риска развития гипогликемии. В связи с риском развития гипогликемии следует соблюдать осторожность при назначении трехкомпонентной комбинации препарата Випидия с метформином и тиазолидиндионом. В случае развития гипогликемии возможно рассмотреть уменьшение дозы метформина или тиазолидиндиона. Эффективность и безопасность алоглиптина при приеме в тройной комбинации с метформином и производным сульфонилмочевины не исследовались. Пациенты с почечной недостаточностью Пациентам с легкой почечной недостаточностью (клиренс креатинина от >:50 до 80 мл/мин) коррекции дозы препарата Випидия не требуется. У пациентов с почечной недостаточностью средней степени тяжести (клиренс креатинина от 30 до 50 мл/мин) доза препарата Випидия составляет 12,5 мг один раз в сутки. Алоглиптин не должен применяться у пациентов с тяжелой почечной недостаточностью и пациентов с терминальной стадией почечной недостаточности, нуждающихся в гемодиализе (клиренс креатинина от <:30 мл/мин). Пациентам с почечной недостаточностью рекомендуется проводить оценку функции почек до начала лечения препаратом Випидия и периодически в процессе лечения. Пациенты с печеночной недостаточностью Не требуется коррекции дозы препарата Випидия у пациентов с печеночной недостаточностью легкой и средней степени тяжести (от 5 до 9 баллов по шкале Чайлда-Пью). Препарат не исследовался у пациентов с тяжелой печеночной недостаточностью (более 9 баллов по шкале Чайлда-Пью), поэтому он не должен применяться у данной группы пациентов. Пациенты старше 65 лет Не требуется коррекции дозы препарата Випидия у пациентов старше 65 лет. Тем не менее следует особенно тщательно подбирать дозу алоглиптина в связи с потенциальной возможностью снижения функции почек у данной группы пациентов. Побочные эффекты и передозировка Побочные эффекты: Частота побочных эффектов препарата расценивается следующим образом:Очень частые: 1/10. Частые: 1/100, <: 1/10. Нечастые: 1/1000, <: 1/100. Редкие: 1/10 000, <:1/1000. Очень редкие: <: 1/10 000. Частота не установлена (данные постмаркетинговых наблюдений) Нарушения со стороны нервной системы:Часто: головная боль. Нарушения со стороны желудочно-кишечного тракта:Часто: боль в эпигастральной области, гастроэзофагеальная рефлюксная болезнь. Частота не установлена: острый панкреатит. Нарушения со стороны печени и желчевыводящих путей:Частота не установлена: нарушение функции печени, в том числе печеночная недостаточность. Нарушения со стороны кожи и подкожных тканей:Часто: зуд, сыпь. Частота не установлена: эксфолиативные кожные заболевания, включая синдром Стивенса-Джонсона, ангионевротический отек, крапивница. Инфекционные или паразитарные заболевания Часто: инфекции верхних дыхательных путей, назофарингит. Нарушения со стороны иммунной системы. Частота не установлена: реакции гиперчувствительности, включая анафилактическую реакцию. Передозировка: Максимальная доза алоглиптина в клинических исследованиях составляла 800 мг/сут у здоровых добровольцев и 400 мг/сут у пациентов с сахарным диабетом 2 типа в течение 14 дней. Это в 32 и 16 раз, соответственно, превышает рекомендуемую суточную дозу 25 мг алоглиптина. Какие-либо серьезные нежелательные явления при приеме препарата в этих дозах отсутствовали. При передозировке может быть рекомендовано промывание желудка и симптоматическое лечение. Алоглиптин слабо диализируется. В клинических исследованиях только 7 % дозы удалялось из организма в течение 3 часового сеанса диализа. Данных об эффективности перитонеального диализа алоглиптина нет. Взаимодействие с другими ЛС: Влияние других лекарственных препаратов на алоглиптин Алоглиптин в основном выводится из организма в неизмененном виде почками, и в незначительной степени метаболизируется ферментной системой цитохрома (CYP) Р450. В исследованиях по взаимодействию с другими лекарственными средствами на фармакокинетику алоглиптина не оказывали клинически значимого эффекта следующие препараты: гемфиброзил (ингибитор CYP2C8/9), флюконазол (ингибитор CYP2C9), кетоконазол (ингибитор CYP3A4), циклоспорин (ингибитор р-гликопротеина), ингибитор α-гликозидазы, дигоксин, метформин, циметидин, пиоглитазон или аторвастатин. Влияние алоглиптина на другие лекарственные препараты В исследованиях in vitro показано, что алоглиптин не ингибирует и не индуцирует изоформы CYP 450 в концентрациях, достигаемых при приеме алоглиптина в рекомендуемой дозе 25 мг. Взаимодействия с изоформами CYP 450 не ожидается, и выявлено не было. В исследованиях in vitro выявлено, что алоглиптин не является ни субстратом, ни ингибитором ОАТ1, ОАТ3 и ОСТ2. Кроме того, данные клинических исследований не указывают на взаимодействие с ингибиторами или субстратами р-гликопротеина. В клинических исследованиях по взаимодействию с другими лекарственными средствами алоглиптин не оказывал клинически значимого влияния на фармакокинетику следующих препаратов: кофеина, (R)- и (S)- варфарина, пиоглитазона, глибенкламида, толбутамида, декстрометорфана, аторвастатина, мидазолама, пероральных контрацептивов (норэтиндрон и этинилэстрадиол), дигоксина, фексофенадина, метформина или циметидина. Основываясь на этих данных, алоглиптин не ингибирует изоферменты системы цитохрома CYP1A2, CYP3A4, CYP2D6, CYP2C9, р-гликопротеин и ОСТ2. Алоглиптин не оказывал воздействия на протромбиновый индекс или Международное нормализованное отношение (МНО) у здоровых добровольцев при одновременном приеме с варфарином. Прием алоглиптина в комбинации с метформином, или пиоглитазоном (тиазолидиндион), или ингибитором α-гликозидазы, или глибенкламидом (производное сульфонилмочевины) не показал клинически значимых фармакокинетических взаимодействий. Фармакологическое действие и фармакокинетика Алоглиптин является сильнодействующим и высокоселективным ингибитором ДПП-4. Его избирательность в отношении ДПП-4 более чем в 10 000 раз превосходит его действие в отношении других родственных ферментов, включая ДПП-8 и ДПП-9. ДПП-4 является основным ферментом, участвующим в быстром разрушении гормонов семейства инкретинов: глюкагоноподобного пептида-1 (ГПП-1) и глюкозозависимого инсулинотропного полипептида (ГИП). Гормоны семейства инкретинов секретируются в кишечнике, их концентрация повышается в ответ на прием пищи. ГПП-1 и ГИП увеличивают синтез инсулина и его секрецию бета-клетками поджелудочной железы. ГПП-1 также ингибирует секрецию глюкагона и уменьшает продукцию глюкозы печенью. Поэтому повышая концентрацию инкретинов, алоглиптин увеличивает глюкозозависимую секрецию инсулина и уменьшает секрецию глюкагона при повышенной концентрации глюкозы в крови. У пациентов с сахарным диабетом 2 типа с гипергликемией эти изменения секреции инсулина и глюкагона приводят к снижению концентрации гликозилированного гемоглобина НbА1с и уменьшению концентрации глюкозы в плазме крови как натощак, так и постпрандиальной глюкозы. Фармакокинетика: Фармакокинетика алоглиптина схожа у здоровых лиц и у пациентов с сахарным диабетом 2 типа. Всасывание Абсолютная биодоступность алоглиптина составляет приблизительно 100 %. Одновременный прием с пищей с высоким содержанием жиров не оказывал влияние на площадь под кривой "концентрация-время" (AUC) алоглиптина, поэтому его можно принимать вне зависимости от приема пищи. У здоровых лиц после однократного перорального приема до 800 мг алоглиптина отмечается быстрая абсорбция препарата с достижением средней максимальной концентрации (среднее ТСmах) в интервале от 1 до 2 часов с момента приема. Ни у здоровых добровольцев, ни у пациентов с сахарным диабетом 2 типа не наблюдалось клинически значимой кумуляции алоглиптина после многократного приема. AUC алоглиптина пропорционально увеличивается при однократном приеме в терапевтическом диапазоне доз от 6,25 мг до 100 мг. Коэффициент вариабельности AUC алоглиптина среди пациентов небольшой (17 %). AUC (0-inf) алоглиптина после однократного приема была схожа с AUC (0-24) после приема такой же дозы один раз в сутки в течение 6 дней. Это указывает на отсутствие временной зависимости в кинетике алоглиптина после многократного приема. Распределение После однократного внутривенного введения алоглиптина в дозе 12,5 мг у здоровых добровольцев объем распределения в терминальной фазе составлял 417 л, что указывает на то, что алоглиптин хорошо распределяется в тканях. Связь с белками плазмы составляет примерно 20-30 %. Метаболизм Алоглиптин не подвергается интенсивному метаболизму, от 60 до 70 % алоглиптина выводится в неизмененном виде почками. После введения 14С-меченного алоглиптина внутрь были определены два основных метаболита: N-деметилированный алоглиптин, М-I (<: 1 % исходного вещества), и N-ацетилированный алоглиптин, М-II (<: 6 % исходного вещества). М-I является активным метаболитом и высокоселективным ингибитором ДПП-4, схожим по действию с самим алоглиптином: М-II не проявляет ингибирующую активность по отношению к ДПП-4 или другим ДПП ферментам. В исследованиях in vitro было выявлено, что CYP2D6 и CYP3A4 участвуют в ограниченном метаболизме алоглиптина. Также исследования in vitro показывают, что алоглиптин не индуцирует CYP1A2, CYP2C9, CYP2B6 и не ингибирует CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 или CYP3A4 в концентрациях, достигаемых при рекомендуемой дозе 25 мг алоглиптина. В условиях in vitro алоглиптин может в небольшой степени индуцировать CYP3A4, однако в условиях in vivo алоглиптин не индуцирует CYP3A4. Алоглиптин не ингибирует почечные транспортеры органических анионов человека первого (ОАТ1), третьего (ОАТЗ) типов и почечные транспортеры органических катионов человека второго (ОСТ2) типа. Алоглиптин существует преимущественно в виде (R)-энантиомера (>: 99 %) и в условиях in vivo или в небольших количествах, или вообще не подвергается хиральному преобразованию в (S)-энантиомер. (S)-энантиомер не обнаруживается при приеме алоглиптина в терапевтических дозах. Выведение После перорального приема 14С-меченного алоглиптина 76 % общей радиоактивности было выведено почками и 13 % - через кишечник. Средний почечный клиренс алоглиптина (170 мл/мин) больше, чем средняя скорость клубочковой фильтрации (около 120 мл/мин), что позволяет предположить, что алоглиптин частично выводится за счет активной почечной экскреции. Средний терминальный период полувыведения алоглиптина (Т1/2) составляет приблизительно 21 ч. Фармакокинетика у отдельных групп пациентов Пациенты с почечной недостаточностью Исследование алоглиптина в дозе 50 мг в сутки было проведено у пациентов с различной степенью тяжести хронической почечной недостаточности. Включенные в исследование пациенты были разделены на 4 группы в соответствии с формулой Кокрофта-Голта: пациенты с легкой (клиренс креатинина от 50 до 80 мл/мин), средней степени тяжести (клиренс креатинина от 30 до 50 мл/мин) и тяжелой почечной недостаточностью (клиренс креатинина менее 30 мл/мин), а также пациенты с терминальной стадией хронической почечной недостаточности, нуждающиеся в гемодиализе. AUC алоглиптина у пациентов с легкой почечной недостаточностью увеличивалась приблизительно в 1,7 раз по сравнению с контрольной группой. Тем не менее данное увеличение AUC находилось в пределах допустимого отклонения для контрольной группы, поэтому коррекция дозы препарата у таких пациентов не требуется (см. Способ применения и дозы). Увеличение AUC алоглиптина приблизительно в два раза по сравнению с контрольной группой отмечалось у пациентов с почечной недостаточностью средней степени тяжести. Приблизительно четырехкратное увеличение AUC отмечалось у пациентов с тяжелой почечной недостаточностью, а также у пациентов с терминальной стадией хронической почечной недостаточности по сравнению с контрольной группой. (Пациентам с терминальной стадией почечной недостаточности проводили гемодиализ сразу же после приема алоглиптина. Около 7 % дозы удалялось из организма в течение 3-х часового сеанса диализа.) Таким образом, для достижения терапевтической концентрации алоглиптина в плазме крови, сходной с таковой у пациентов с нормальной функцией почек, необходима коррекция дозы у пациентов с почечной недостаточностью средней степени тяжести (см. Способ применения и дозы). Алоглиптин не рекомендуется принимать пациентам с тяжелой почечной недостаточностью, а также с терминальной стадией почечной недостаточности, требующей проведения гемодиализа. Пациенты с печеночной недостаточностью У пациентов со средней степенью тяжести печеночной недостаточности AUC и Сmах алоглиптина уменьшаются приблизительно на 10 % и 8 %, соответственно, по сравнению с пациентами с нормальной функцией печени. Данные значения клинически не значимы. Таким образом, коррекция дозы препарата при легкой и средней степени тяжести печеночной недостаточности (от 5 до 9 баллов по шкале Чайлд-Пью) не требуется. Нет клинических данных о применении алоглиптина у пациентов с тяжелой печеночной недостаточностью (более 9 баллов по шкале Чайлд-Пью, см. Способ применения и дозы). Другие группы пациентов Возраст (65-81 лет), пол, раса, масса тела пациентов не оказывали клинически значимого воздействия на фармакокинетические параметры алоглиптина. Коррекции дозы препарата не требуется (см. Способ применения и дозы). Фармакокинетика у детей до 18 лет не исследовалась. Особые указания Применение с другими гипогликемическими препаратами С целью уменьшения риска развития гипогликемии рекомендуется снижение дозы производных сульфонилмочевины, инсулина или комбинации пиоглитазона (тиазолидиндиона) с метформином при одновременном применении с препаратом Випидия (см. Способ применения и дозы). Неизученные комбинации Эффективность и безопасность применения препарата Випидия в комбинации с ингибиторами натрий-зависимых котранспортеров глюкозы 2 или аналогами глюкагоноподобного пептида и в тройной комбинации с метформином и производными сульфонилмочевины не исследовались. Почечная недостаточность Т.к. пациентам с почечной недостаточностью средней степени тяжести требуется проводить коррекцию дозы препарата Випидия, рекомендуется проводить оценку функции почек до начала и периодически в течение лечения (см. Способ применения и дозы). Препарат Випидия не должен применяться у пациентов с тяжелой почечной недостаточностью, а также у пациентов с терминальной стадией хронической почечной недостаточностью, требующей гемодиализа (см. Способ применения и дозы). Острый панкреатит Применение ингибиторов ДПП-4 связано с потенциальным риском развития острого панкреатита. В обобщенном анализе 13 клинических исследований применения алоглиптина в дозе 25 мг/сут, 12,5 мг/сут, препарата сравнения и плацебо частота развития острого панкреатита составила 3, 1, 1 или 0 случаев на 1000 пациенто-лет в каждой группе соответственно. Пациенты должны быть проинформированы о характерных симптомах острого панкреатита: стойкая сильная боль в животе, которая может иррадиировать в спину. При подозрении на развитие острого панкреатита прием препарата Випидия прекращают: при подтверждении острого панкреатита прием препарат не возобновляют. Нет данных о том, существует ли повышенный риск развития панкреатита на фоне приема препарата Випидия у пациентов с панкреатитом в анамнезе. Поэтому пациентам с панкреатитом в анамнезе следует соблюдать осторожность. Печеночная недостаточность Были получены постмаркетинговые сообщения о нарушениях функции печени, включая печеночную недостаточность при приеме алоглиптина. Их связь с применением препарата не была установлена. Однако пациентов необходимо тщательно обследовать на наличие возможных отклонений функции печени. Если обнаружены отклонения в функции печени и альтернативная этиология их возникновения не установлена, следует рассмотреть возможность прекращения лечения препаратом. Влияние на способность управлять транспортными средствами: Препарат Випидия не оказывает или оказывает незначительное влияние на способность управлять транспортными средствами и механизмами. Тем не менее необходимо учитывать риск развития гипогликемии при применении препарата в сочетании с другими гипогликемическими препаратами (производные сульфонилмочевины, инсулин или комбинированная терапия с пиоглитазоном и метформином) и соблюдать осторожность при управлении транспортными средствами и механизмами. Условия хранения и отпуска из аптек Условия хранения:Хранить при температуре не выше 25 °С. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Випидия Международное непатентованное название:Алоглиптин. Форма выпуска:таблетки, покрытые пленочной оболочкой. Состав:1 таблетка 12,5 мг содержит Активное вещество: алоглиптина бензоат - 17 мг (в пересчете на алоглиптин - 12,5 мг). Вспомогательные вещества: Ядро: маннитол 96,7 мг, целлюлоза микрокристаллическая 22,5 мг, гипролоза 4,5 мг, кроскармеллоза натрия 7,5 мг, магния стеарат 1,8 мг. Пленочная оболочка: гипромеллоза 2910 5,34 мг, титана диоксид 0,6 мг, краситель железа оксид желтый 0,06 мг, макрогол-8000 следовые количества, чернила серые F1 следовые количества 1. 1 Чернила серые F1 содержат: шеллак 26 %, краситель железа оксид черный 10%, этанол 26 %, бутанол 38 %. 1 таблетка 25 мг содержит Активное вещество: алоглиптина бензоат - 34 мг (в пересчете на алоглиптин - 25 мг). Вспомогательные вещества: Ядро: маннитол 79,7 мг, целлюлоза микрокристаллическая 22,5 мг, гипролоза 4,5 мг, кроскармеллоза натрия 7,5 мг, магния стеарат 1,8 мг. Пленочная оболочка: гипромеллоза 2910 5,34 мг, титана диоксид 0,6 мг, краситель железа оксид красный 0,06 мг, макрогол-8000 следовые количества, чернила серые F1 следовые количества. 1 Чернила серые F1 содержат: шеллак 26 %, краситель железа оксид черный 10%, этанол 26 %, бутанол 38 %. АТХ: Регистрация: Лекарственное средство ЛП-002644 Фармгруппа: Гипогликемическое средство - дипептидилпептидазы-4 ингибитор (ДПП-4)Дата регистрации: 08.10.2014. Окончание регстрации: . Описание:Дозировка 12,5 мг Овальные двояковыпуклые таблетки, покрытые пленочной оболочкой желтого цвета, с нанесенными чернилами надписями "ТАК" и "ALG-12.5" на одной стороне. Дозировка 25 мг Овальные двояковыпуклые таблетки, покрытые пленочной оболочкой светло-красного цвета, с нанесенными чернилами надписями "ТАК" и "ALG-25" на одной стороне. Упаковка:Таблетки покрытые пленочной оболочкой 12,5 мг и 25 мг. По 7 таблеток в Ал/Ал блистер, по 4 блистера вместе с инструкцией по применению помещают в картонную пачку. Срок годности:3 года. Не применять по истечении срока годности. Владелец рег.удостоверения:Такеда Фармасьютикалс США, Инк. Производитель:TAKEDA IRELAND, Ltd. Представительство:Такеда Фармасьютикалс ООО
Модель:
RUR 229
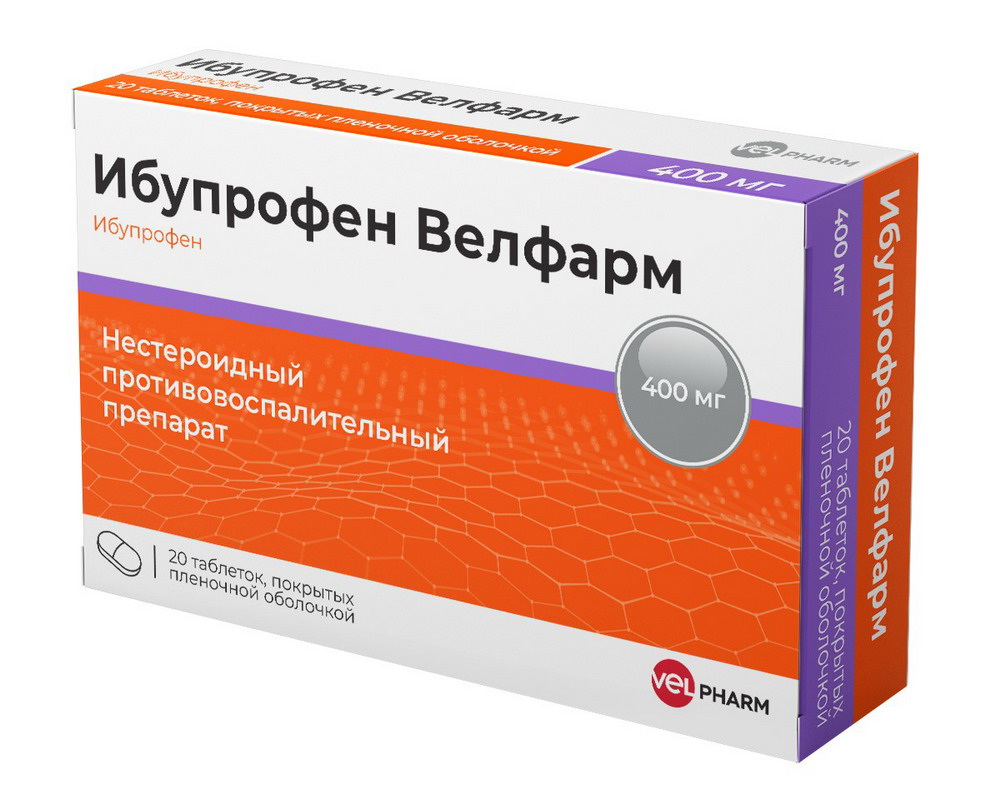
Применяют при головной боли, мигрени, зубной боли, болезненных менструациях, невралгии, боли в спине, мышечной боли, ревматической боли и боли в суставах; а также при лихорадочном состоянии при гриппе и простудных заболеваниях. Состав: Действующее вещество: ибупрофен – 200,0 мг, 400,0 мг; Вспомогательные вещества: повидон К90 (коллидон 90 F), целлюлоза микрокристаллическая МС-101, тальк, кросповидон (коллидон ЦЛ, коллидон CL-M), кальция стеарат, кремния диоксид коллоидный (аэросил), крахмал кукурузный. Состав оболочки: [сухая смесь для пленочного покрытия, содержащая гипромеллозу, титана диоксид, макрогол или гипромеллоза (оксипропилметилцеллюлоза), титана диоксид, макрогол 6000 (полиэтиленгликоль 6000, полиэтиленоксид 6000)]. Способ применения и дозы: Взрослые, пожилые и дети старше 12 лет по 200 мг (1 таблетка) 3-4 раза в сутки. Суточная доза составляет 1200 мг (не принимать больше 6 таблеток по 200 мг) в течение 24 ч. Таблетки следует проглатывать, запивая водой, лучше во время или после еды. Не принимать чаще, чем через 4 часа. Не превышайте указанной дозы! Курс лечения без консультации врача не должен превышать 5 дней. Если симптомы сохраняются, проконсультируйтесь с врачом. Не применять у детей моложе 12 лет без консультации врача. Детям с 6 до 12 лет (с массой тела более 20 кг): по 1 таблетке 200 мг не более 4 раз в день. Интервал между приёмом таблеток не менее 6 часов. Противопоказания: Гиперчувствительность к ибупрофену или любому из компонентов, входящих в состав препарата; Полное или неполное сочетание бронхиальной астмы, рецидивирующего полипоза носа и околоносовых пазух, и непереносимости ацетилсалициловой кислоты или других НПВП (в том числе в анамнезе); Эрозивно-язвенные заболевания органов желудочно-кишечного тракта (в том числе язвенная болезнь желудка и двенадцатиперстной кишки, болезнь Крона, язвенный колит) или язвенное кровотечение в активной фазе или в анамнезе (два или более подтвержденных эпизода язвенной болезни или язвенного кровотечения); Кровотечение или перфорация язвы желудочно-кишечного тракта в анамнезе, спровоцированные применением НПВП; Тяжелая сердечная недостаточность (класс IV по NYHA – классификация Нью-Йоркской Ассоциации кардиологов); Тяжелая печеночная недостаточность или заболевание печени в активной фазе; Почечная недостаточность тяжелой степени тяжести (клиренс креатинина < 30 мл/мин), подтвержденная гиперкалиемия; Декомпенсированная сердечная недостаточность; период после проведения аортокоронарного шунтирования; Цереброваскулярное или иное кровотечение; Гемофилия и другие нарушения свертываемости крови (в том числе гипокоагуляция), геморрагические диатезы; Беременность в сроке более 20 недель; Детский возраст: до 6 лет – для таблеток 200 мг; до 12 лет – для таблеток 400 мг

Модель:
RUR 1017
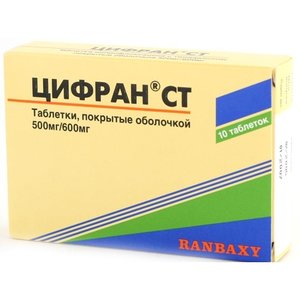
Состав Противопоказания Дозировка Показания к применению Взаимодействие с другими лекарственными средствами Передозировка Фармакологическое действие Беременность и кормление грудью Условия отпуска из аптек Побочные явления Особые указания Условия хранения Способ применения и дозы Информация Состав Активное вещество: 1 таблетка 12,5 мг содержит: алоглиптина бензоат 17 мг (в пересчете на алоглиптин 12,5 мг). 1 таблетка 25 мг содержит: алоглиптина бензоат 34 мг (в пересчете на алоглиптин 25 мг). Вспомогательные вещества: 1 таблетка 12,5 мг содержит: Ядро: маннитол 96,7 мг, целлюлоза микрокристаллическая 22,5 мг, гипролоза 4,5 мг, кроскармеллоза натрия 7,5 мг, магния стеарат 1,8 мг. Пленочная оболочка: гипромеллоза 2910 5,34 мг, титана диоксид 0,6 мг, краситель железа оксид желтый 0,06 мг, макрогол-8000 cледовые количества, чернила серые F1 cледовые количества. 1 таблетка 25 мг содержит: Ядро: маннитол 79,7 мг, целлюлоза микрокристаллическая 22,5 мг, гипролоза 4,5 мг, кроскармеллоза натрия 7,5 мг, магния стеарат 1,8 мг. Пленочная оболочка: гипромеллоза 2910 5,34 мг, титана диоксид 0,6 мг, краситель железа оксид красный 0,06 мг, макрогол-8000 следовые количества, чернила серые F1 следовые количества Чернила серые F1 содержат: шеллак 26 %, краситель железа оксид черный 10%, этанол 26 %, бутанол 38 %. Описание: Дозировка 12,5 мг Овальные двояковыпуклые таблетки, покрытые пленочной оболочкой желтого цвета, с нанесенными чернилами надписями «ТАК» и «ALG-12.5» на одной стороне. Дозировка 25 мг Овальные двояковыпуклые таблетки, покрытые пленочной оболочкой светло-красного цвета, с нанесенными чернилами надписями «ТАК» и «ALG-25» на одной стороне. Форма выпуска: Таблетки, покрытые пленочной оболочкой, 12,5 мг и 25 мг. По 14 таблеток в Ал/Ал блистер, по 2 блистера вместе с инструкцией по применению помещают в картонную пачку. Противопоказания Повышенная чувствительность к алоглиптину или к любому вспомогательному веществу, или серьезные реакции гиперчувствительности к любому ДПП-4 ингибитору в анамнезе, в том числе анафилактические реакции, анафилактический шок и ангионевротический отек; сахарный диабет 1 типа; диабетический кетоацидоз; хроническая сердечная недостаточность (функциональный класс III-IV по функциональной классификации хронической сердечной недостаточности Нью- Йоркской кардиологической ассоциации); тяжелая печеночная недостаточность (более 9 баллов по шкале Чайлд-Пью) из-за отсутствия клинических данных о применении; тяжелая почечная недостаточность; беременность, период грудного вскармливания - в связи с отсутствием клинических данных по применению; детский возраст до 18 лет - в связи с отсутствием клинических данных по применению. C осторожностью Острый панкреатит в анамнезе (см. Особые указания). У пациентов с почечной недостаточностью средней степени тяжести (см. Особые указания). В комбинации с производным сульфонилмочевины или инсулином (см. Особые указания). Прием трехкомпонентной комбинации препарата Випидия® с метформином и тиазолидиндионом (см. Особые указания). Дозировка 12,5 мг Показания к применению Сахарный диабет 2 типа для улучшения гликемического контроля при неэффективности диетотерапии и физических нагрузок: у взрослых в качестве монотерапии, в сочетании с другими пероральными гипогликемическими средствами или с инсулином. Взаимодействие с другими лекарственными средствами Влияние других лекарственных препаратов на алоглиптин Алоглиптин в основном выводится из организма в неизмененном виде почками и в незначительной степени метаболизируется ферментной системой цитохрома (CYP) Р450. В исследованиях по взаимодействию с другими лекарственными средствами на фармакокинетику алоглиптина не оказывали клинически значимого эффекта следующие препараты: гемфиброзил (ингибитор CYP2С8/9), флюконазол (ингибитор CYP2С9), кетоконазол (ингибитор CYP3А4), циклоспорин (ингибитор p-гликопротеина), ингибитор а-гликозидазы, дигоксин, метформин, циметидин, пиоглитазон или аторвастатин Влияние алоглиптина на другие лекарственные препараты В исследованиях in vitro показано, что алоглиптин не ингибирует и не индуцирует изоформы CYP 450 в концентрациях, достигаемых при приеме алоглиптина в рекомендуемой дозе 25 мг. Взаимодействия с изоформами CYP 450 не ожидается и выявлено не было. В исследованиях in vitro выявлено, что алоглиптин не является ни субстратом, ни ингибитором ОАТ1, ОАТ3 и ОСТ2. Кроме того, данные клинических исследований не указывают на взаимодействие с ингибиторами или субстратами р-гликопротеина. В клинических исследованиях по взаимодействию с другими лекарственными средствами алоглиптин не оказывал клинически значимого влияния на фармакокинетику следующих препаратов: кофеина, (R)- и (S)-варфарина, пиоглитазона, глибенкламида, толбутамида, декстрометорфана, аторвастатина, мидазолама, пероральных контрацептивов (норэтиндрон и этинилэстрадиол), дигоксина, фексофенадина, метформина или циметидина. Основываясь на этих данных, алоглиптин не ингибирует изоферменты системы цитохрома CYP1А2, CYP3А4, CYP2D6, CYP2С9, р-гликопротеин и ОСТ2. Алоглиптин не оказывал воздействия на протромбиновый индекс или Международное нормализованное отношение (МНО) у здоровых добровольцев при одновременном приеме с варфарином. Прием алоглиптина в комбинации с метформином, или пиоглитазоном (тиазолидиндион), или ингибитором альфа-гликозидазы, или глибенкламидом (производное сульфонилмочевины) 10 не показал клинически значимых фармакокинетических взаимодействий. Передозировка Максимальная доза алоглиптина в клинических исследованиях составляла 800 мг/сут у здоровых добровольцев и 400 мг/сут у пациентов с сахарным диабетом 2 типа в течение 14 дней. Это в 32 и 16 раз соответственно превышает рекомендуемую суточную дозу 25 мг алоглиптина. Какие-либо серьезные нежелательные явления при приеме препарата в этих дозах отсутствовали. При передозировке может быть рекомендовано промывание желудка и симптоматическое лечение. Алоглиптин слабо диализируется. В клинических исследованиях только 7 % дозы удалялось из организма в течение 3 часового сеанса диализа. Данных об эффективности перитонеального диализа алоглиптина нет. Фармакологическое действие Фармакологическая группа: Гипогликемическое средство – дипептидилпептидазы-4 ингибитор (ДПП-4). Фармакодинамика: Алоглиптин является сильнодействующим и высокоселективным ингибитором ДПП-4. Его избирательность в отношении ДПП-4 более чем в 10 000 раз превосходит его действие в отношении других родственных ферментов, включая ДПП-8 и ДПП-9. ДПП-4 является основным ферментом, участвующим в быстром разрушении гормонов семейства инкретинов: глюкагоноподобного пептида-1 (ГПП-1) и глюкозозависимого инсулинотропного полипептида (ГИП). Гормоны семейства инкретинов секретируются в кишечнике, их концентрация повышается в ответ на прием пищи. ГПП-1 и ГИП увеличивают синтез инсулина и его секрецию бета-клетками поджелудочной железы. ГПП-1 также ингибирует секрецию глюкагона и уменьшает продукцию глюкозы печенью. Поэтому, повышая концентрацию инкретинов, алоглиптин увеличивает глюкозозависимую секрецию инсулина и уменьшает секрецию глюкагона при повышенной концентрации глюкозы в крови. У пациентов с сахарным диабетом 2 типа с гипергликемией эти изменения секреции инсулина и глюкагона приводят к снижению концентрации гликозилированного гемоглобина HbA1с и уменьшению концентрации глюкозы в плазме крови как натощак, так и постпрандиально. Фармакокинетика: Фармакокинетика алоглиптина схожа у здоровых лиц и у пациентов с сахарным диабетом 2 типа. Всасывание Абсолютная биодоступность алоглиптина составляет приблизительно 100 %. Одновременный прием с пищей с высоким содержанием жиров не оказывал влияние на площадь под кривой «концентрация-время» (AUC) алоглиптина, поэтому его можно принимать вне зависимости от приема пищи. У здоровых лиц после однократного перорального приема до 800 мг алоглиптина отмечается быстрая абсорбция препарата с достижением средней максимальной концентрации (среднее ТСmax. ) в интервале от 1 до 2 часов с момента приема. Ни у здоровых добровольцев, ни у пациентов с сахарным диабетом 2 типа не наблюдалось клинически значимой кумуляции алоглиптина после многократного приема. AUC алоглиптина пропорционально увеличивается при однократном приеме в терапевтическом диапазоне доз от 6,25 мг до 100 мг. Коэффициент вариабельности AUC алоглиптина среди пациентов небольшой (17 %). AUC (0-inf) алоглиптина после однократного приема была схожа с AUC (0-24) после приема такой же дозы один раз в сутки в течение 6 дней. Это указывает на отсутствие временной зависимости в кинетике алоглиптина после многократного приема Распределение После однократного внутривенного введения алоглиптина в дозе 12,5 мг у здоровых добровольцев объем распределения в терминальной фазе составлял 417 л, что указывает на то, что алоглиптин хорошо распределяется в тканях. Связь с белками плазмы составляет примерно 20-30 %. Метаболизм Алоглиптин не подвергается интенсивному метаболизму, от 60 до 70 % алоглиптина выводится в неизмененном виде почками. После введения 14С-меченного алоглиптина внутрь были определены два основных метаболита: N-деметилированный алоглиптин, M-I (< 1 % исходного вещества), и Nацетилированный алоглиптин, M-II (< 6 % исходного вещества). M-I является активным метаболитом и высокоселективным ингибитором ДПП-4, схожим по действию с самим алоглиптином; M-II не проявляет ингибирующую активность по отношению к ДПП-4 или другим ДПП ферментам. В исследованиях in vitro было выявлено, что CYP2D6 и CYP3A4 участвуют в ограниченном метаболизме алоглиптина. Также исследования in vitro показывают, что алоглиптин не индуцирует CYP1A2, CYP2C9, CYP2B6 и не ингибирует CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 или CYP3A4 в концентрациях, достигаемых при рекомендуемой дозе 25 мг алоглиптина. В условиях in vitro алоглиптин может в небольшой степени индуцировать CYP3A4, однако в условиях in vivo алоглиптин не индуцирует CYP3A4. Алоглиптин не ингибирует почечные транспортеры органических анионов человека первого (ОАТ1), третьего (ОАТ3) типов и почечные транспортеры органических катионов человека второго (ОСТ2) типа. Алоглиптин существует преимущественно в виде (R)-энантиомера (> 99 %) и в условиях in vivo или в небольших количествах, или вообще не подвергается хиральному преобразованию в (S)-энантиомер. (S)-энантиомер не обнаруживается при приеме алоглиптина в терапевтических дозах. Выведение После перорального приема 14С-меченного алоглиптина 76 % общей радиоактивности было выведено почками и 13 % - через кишечник. Средний почечный клиренс алоглиптина (170 мл/мин) больше, чем средняя скорость клубочковой фильтрации (около 120 мл/мин), что позволяет предположить, что алоглиптин частично выводится за счет активной почечной экскреции. Средний терминальный период полувыведения алоглиптина (Т1/2) составляет приблизительно 21 ч. Фармакокинетика у отдельных групп пациентов Пациенты с почечной недостаточностью Исследование алоглиптина в дозе 50 мг в сутки было проведено у пациентов с различной степенью тяжести хронической почечной недостаточности. Включенные в исследование пациенты были разделены на 4 группы в соответствии с формулой Кокрофта-Голта: пациенты с легкой (клиренс креатинина от 50 до 80 мл/мин), средней степенью тяжести (клиренс креатинина от 30 до 50 мл/мин) и тяжелой почечной недостаточностью (клиренс креатинина менее 30 мл/мин), а также пациенты с терминальной стадией хронической почечной недостаточности, нуждающиеся в гемодиализе. AUC алоглиптина у пациентов с легкой почечной недостаточностью увеличивалась приблизительно в 1,7 раз по сравнению с контрольной группой. Тем не менее данное увеличение AUC находилось в пределах допустимого отклонения для контрольной группы, поэтому коррекция дозы препарата у таких пациентов не требуется (см. Способ применения и дозы). Увеличение AUC алоглиптина приблизительно в два раза по сравнению с контрольной группой отмечалось у пациентов с почечной недостаточностью средней степени тяжести. Приблизительно четырехкратное увеличение AUC отмечалось у пациентов с тяжелой почечной недостаточностью, а также у пациентов с терминальной стадией хронической почечной недостаточности по сравнению с контрольной группой. (Пациентам с терминальной стадией почечной недостаточности проводили гемодиализ сразу же после приема алоглиптина. Около 7 % дозы удалялось из организма в течение 3-х часового 5 сеанса диализа. ) Таким образом, для достижения терапевтической концентрации алоглиптина в плазме крови, сходной с таковой у пациентов с нормальной функцией почек, необходима коррекция дозы у пациентов с почечной недостаточностью средней степени тяжести (см. Способ применения и дозы). Алоглиптин не рекомендуется принимать пациентам с тяжелой почечной недостаточностью, а также с терминальной стадией почечной недостаточности, требующей проведения гемодиализа. Пациенты с печеночной недостаточностью У пациентов со средней степенью тяжести печеночной недостаточности AUC и Сmax. алоглиптина уменьшаются приблизительно на 10 % и 8 % соответственно, по сравнению с пациентами с нормальной функцией печени. Данные значения клинически не значимы. Таким образом, коррекция дозы препарата при легкой и средней степени тяжести печеночной недостаточности (от 5 до 9 баллов по шкале Чайлд-Пью) не требуется. Нет клинических данных о применении алоглиптина у пациентов с тяжелой печеночной недостаточностью (более 9 баллов по шкале Чайлд-Пью, см. Способ применения и дозы). Другие группы пациентов Возраст (65-81 лет), пол, раса, масса тела пациентов не оказывали клинически значимого воздействия на фармакокинетические параметры алоглиптина. Коррекции дозы препарата не требуется (см. Способ применения и дозы). Фармакокинетика у детей до 18 лет не исследовалась. Беременность и кормление грудью Не проводилось исследований применения алоглиптина у беременных женщин. Исследования на животных не показали прямого или непрямого негативного воздействия алоглиптина на репродуктивную систему. Однако в целях предосторожности применение препарата Випидия® во время беременности противопоказано. Отсутствуют данные о проникновении алоглиптина в грудное молоко у людей. Исследования на животных показали, что алоглиптин проникает в грудное молоко, поэтому нельзя исключить риск возникновения побочных эффектов у грудных детей. В связи с этим применение препарата в период грудного вскармливания противопоказано. Условия отпуска из аптек По рецепту. Побочные явления Частота побочных эффектов препарата расценивается следующим образом: Очень частые: >1/10 Частые: > 1/100, 1/1000, < 1/100 Редкие: >1/10 000, < 1/1000 Очень редкие: > 1/10 000 Частота не установлена (данные постмаркетинговых наблюдений) Нарушения со стороны нервной системы: часто-головная боль. Нарушения со стороны желудочно-кишечного тракта: часто-боль в эпигастральной области, гастроэзофагеальная рефлюксная болезнь; частота не установлена-острый панкреатит. Нарушения со стороны печени и желчевыводящих путей: частота не установлена-нарушение функции печени, в том числе печеночная недостаточность. Нарушения со стороны кожи и подкожных тканей: часто-зуд, сыпь; частота не установлена-эксфолиативные кожные заболевания, включая синдром Стивенса-Джонсона, полиморфная эритема, ангионевротический отек, крапивница Инфекционные или паразитарные заболевания: часто-инфекции верхних дыхательных путей, назофарингит. Нарушения со стороны иммунной системы: частота не установлена-реакции гиперчувствительности, включая анафилактическую реакцию. Особые указания Применение с другими гипогликемическими препаратами С целью уменьшения риска развития гипогликемии рекомендуется снижение дозы производных сульфонилмочевины, инсулина или комбинации пиоглитазона (тиазолидиндиона) с метформином при одновременном применении с препаратом Випидия® (см. Способ применения и дозы). Неизученные комбинации Эффективность и безопасность применения препарата Випидия® в комбинации с ингибиторами натрий-зависимых котранспортеров глюкозы 2 или аналогами глюкагоноподобного пептида и в тройной комбинации с метформином и производными сульфонилмочевины не исследовались. Почечная недостаточность Т.к. пациентам с почечной недостаточностью средней степени тяжести требуется проводить коррекцию дозы препарата Випидия®, рекомендуется проводить оценку функции почек до начала и периодически в течение лечения (см. Способ применения и дозы). Опыт применения алоглиптина у пациентов, находящихся на гемодиализе, ограничен. Препарат Випидия® не должен применяться у пациентов с тяжелой почечной недостаточностью, а также у пациентов с терминальной стадией хронической почечной недостаточностью, требующей гемодиализа (см. Способ применения и дозы). Алоглиптин не изучался у пациентов, проходящих перитонеальный диализ. Острый панкреатит Применение ингибиторов ДПП-4 связано с потенциальным риском развития острого панкреатита. В обобщенном анализе 13 клинических исследований применения алоглиптина в дозе 25 мг/сут, 12,5 мг/сут, препарата сравнения и плацебо частота развития острого панкреатита составила 2, 1, 1 или 0 случаев на 1000 пациенто-лет в каждой группе соответственно. В исследовании сердечно-сосудистых исходов частота выявления острого панкреатита у пациентов, проходивших лечение алоглиптином или плацебо, составила 3 и 2 случая на 1000 пациенто-лет соответственно. Пациенты должны быть проинформированы о характерных симптомах острого панкреатита: стойкая сильная боль в животе, которая может иррадиировать в спину. При подозрении на развитие острого панкреатита прием препарата Випидия® прекращают; при подтверждении острого панкреатита прием препарат не возобновляют. Нет данных о том, существует ли повышенный риск развития панкреатита на фоне приема препарата Випидия® у пациентов с панкреатитом в анамнезе. Поэтому пациентам с панкреатитом в анамнезе следует соблюдать осторожность. Печеночная недостаточность Были получены постмаркетинговые сообщения о нарушениях функции печени, включая печеночную недостаточность при приеме алоглиптина. Их связь с применением препарата не была установлена. Однако пациентов необходимо тщательно обследовать на наличие возможных отклонений функции печени. Если обнаружены отклонения в функции печени и альтернативная этиология их возникновения не установлена, следует рассмотреть возможность прекращения лечения препаратом. Влияние на способность управлять транспортными средствами и механизмами Препарат Випидия® не оказывает или оказывает незначительное влияние на способность управлять транспортными средствами и механизмами. Тем не менее необходимо учитывать риск развития гипогликемии при применении препарата в сочетании с другими гипогликемическими препаратами (производные сульфонилмочевины, инсулин или комбинированная терапия с пиоглитазоном и метформином) и соблюдать осторожность при управлении транспортными средствами и механизмами. Условия хранения Хранить при температуре не выше 25 C. Хранить в недоступном для детей месте. Способ применения и дозы Препарат принимают внутрь. Рекомендуемая доза препарата Випидия® составляет 25 мг один раз в сутки в качестве монотерапии или в дополнение к метформину, тиазолидиндиону, производным сульфонилмочевины или инсулину, или в качестве трехкомпонентной комбинации с метформином, тиазолидиндионом или инсулином. Препарат Випидия® может приниматься независимо от приема пищи. Таблетки следует проглатывать целиком, не разжевывая, запивая водой. В случае если пациент пропустил прием препарата Випидия®, он должен принять пропущенную дозу как можно быстрее. Недопустим прием двойной дозы препарата Випидия® в один и тот же день. При назначении препарата Випидия® в дополнение к метформину или тиазолидиндиону дозу последних препаратов следует оставить без изменения. При комбинировании препарата Випидия® с производным сульфонилмочевины или инсулином дозу последних целесообразно уменьшить для снижения риска развития гипогликемии. В связи с риском развития гипогликемии следует соблюдать осторожность при назначении трехкомпонентной комбинации препарата Випидия® с метформином и тиазолидиндионом. В случае развития гипогликемии возможно рассмотреть уменьшение дозы метформина или тиазолидиндиона. Эффективность и безопасность алоглиптина при приеме в тройной комбинации с метформином и производным сульфонилмочевины окончательно не установлены. Пациенты с почечной недостаточностью Пациентам с легкой почечной недостаточностью (клиренс креатинина от >50 до 30 до
Модель:
RUR 520
Показания Смешанные бактериальные инфекции, вызванные чувствительными грамположительными и грамотрицательными микроорганизмами, в ассоциации с аэробными и анаэробными микроорганизмами и/или простейшими:заболевания нижних дыхательных путей (острый и хронический (в стадии обострения) бронхит, пневмония, бронхоэктатическая болезнь):инфекции ЛОР-органов (фарингит, тонзиллит, мастоидит, синусит, фронтит, гайморит, средний отит):инфекции ротовой полости (периодонтит, периостит, острый язвенный гингивит):инфекции кожи и мягких тканей (инфицированные язвы, язвенные поражения кожи при "синдроме диабетической стопы", пролежни, раны, ожоги, абсцессы, флегмона):инфекции костей и суставов (септический артрит, остеомиелит):инфекции органов малого таза и половых органов (пельвиоперитонит, тубулярный абсцесс, эндометрит, оофорит, сальпингит, простатит), в том числе в сочетании с трихомониазом:инфекции почек и мочевыводящих путей (пиелонефрит, цистит):инфекции желудочно-кишечного тракта (брюшной тиф, шигеллез, амебиаз):осложненные интраабдоминальные инфекции:профилактика инфекций после хирургических вмешательств. Противопоказания Противопоказания гиперчувствительность к ципрофлоксацину (в том числе к другим фторхинолонам), тинидазолу (в том числе к другим имидазолам) или к любому из компонентов препарата:болезни крови, угнетение костномозгового кроветворения:острая порфирия:органические поражения нервной системы:одновременный прием с тизанидином (риск выраженного снижения артериального давления и наступления выраженной сонливости):детский возраст (до 18 лет):беременность:период лактации:дефицит лактазы, непереносимость лактозы, глюкозо-галактозная мальабсорбция. С осторожностью: Препарат следует с осторожностью применять больным с выраженным атеросклерозом сосудов головного мозга, с нарушениями мозгового кровообращения, с синдромом врожденного удлинения интервала QT, с заболеваниями сердца (сердечная недостаточность, инфаркт миокарда, брадикардия), при электролитном дисбалансе (например, при гипокалиемии, гипомагниемии), при одновременном приеме лекарственных средств, удлиняющих интервал QT (в т. ч. антиаритмические средства IA и III классов), при одновременном применении с ингибиторами изоферментов CYP4501A2 (в т. ч. с теофиллином, метилксантином, кофеином, дулоксетином, клозапином), больным с психическими заболеваниями, эпилепсией, с эпилептическим синдромом, выраженной почечной и/или печеночной недостаточностью, с поражением сухожилий при ранее проводившемся лечении фторхинолонами, пожилой возраст. Беременность Тинидазол может оказывать мутагенное и канцерогенное действие, поэтому применение препарата Цифранв СТ при беременности противопоказано. Тинидазол и ципрофлоксацин экскретируются в грудное молоко, поэтому применение препарата Цифран СТ в период лактации противопоказано. Применение и дозы Внутрь. Препарат следует принимать после еды, запивая достаточным количеством воды. Рекомендуемая доза для взрослых: 1 таблетка 2 раза в день. Продолжительность лечения зависит от тяжести заболевания, но прием препарата всегда должен продолжаться как минимум еще два дня после исчезновения симптомов болезни. Обычно продолжительность лечения составляет 7-10 дней. Таблица рекомендуемых доз препарата для больных с нарушенной функцией почек:Клиренс креатинина Доза>: 60 мл/мин Коррекция дозы не требуется 30-60 мл/мин 300 мг + 250 мг или 600 мг + 500 мг 1 раз в 12 часов<:30 мл/мин 300 мг + 250 мг или 600 мг + 500 мг 1 раз в 24 часа. При назначении препарата пациентам пожилого возраста следует учитывать, что они могут быть более чувствительны к действию препарата вследствие замедленного метаболизма. При гемодиализе или перитонеальном диализе препарат применяется в дозе 300 мг + 250 мг или 600 мг + 500 мг один раз в 24 ч, но принимать препарат следует после сеанса гемодиализа. Побочные эффекты и передозировка Побочные эффекты: Со стороны системы кроветворения: лейкопения, гранулоцитопения, анемия, тромбоцитопения, лейкоцитоз, тромбоцитоз, гемолитическая анемия, нейтропения, агранулоцитоз, панцитопения, угнетение костномозгового кроветворения, вазодилятация, сывороточная болезнь. Со стороны нервной системы: головная боль, головокружение, вертиго, нарушения координации движений (в т. ч. локомоторная атаксия), нарушение походки, дезориентация, повышенная утомляемость, дизартрия, периферическая невропатия, судороги, слабость, тремор, бессонница, "кошмарные" сновидения, тревожность, повышение внутричерепного давления, тромбоз церебральных артерий, спутанность сознания, депрессия, галлюцинации, а также другие проявления психотических реакций (изредка прогрессирующих до состояний, в которых пациент может причинить себе вред), мигрень, обморочные состояния, ажитация, дизестезии, гиперестезия, гипестезии, парестезии, периферическая паралгезия (аномалия восприятия чувства боли), полинейропатия. Со стороны дыхательной системы: нарушения дыхания (включая бронхоспазм). Со стороны органов чувств: нарушения вкуса и обоняния, нарушения зрения (диплопия, изменение цветовосприятия, повышенная светочувствительность), шум в ушах, снижение слуха, потеря слуха. Со стороны сердечно-сосудистой системы: тахикардия, нарушения сердечного ритма, снижение артериального давления, удлинение интервала QT на электрокардиограмме, желудочковые аритмии (в том числе типа "пируэт"). Со стороны пищеварительной системы: снижение аппетита, сухость слизистой оболочки полости рта, "металлический" привкус во рту, тошнота, рвота, диарея, боль в животе, метеоризм, холестатическая желтуха (особенно у пациентов с перенесенными заболеваниями печени), панкреатит, гепатит, гепатонекроз. Со стороны опорно-двигательного аппарата: артралгия, артрит, тендовагинит, разрывы сухожилий, миалгия, повышение мышечного тонуса, мышечная слабость, обострение симптомов миастении. Со стороны мочевыделительной системы: гематурия, кристаллурия (при щелочной моче и снижении диуреза), гломерулонефрит, дизурия, полиурия, задержка мочи, снижение азотовыделительной функции почек, интерстициальный нефрит, почечная недостаточность. Аллергические реакции: кожный зуд, крапивница, образование волдырей,сопровождающихся кровотечениями, и маленьких узелков, образующих струпья, лекарственная лихорадка, точечные кровоизлияния на коже (петехии), отек лица или гортани, отдышка, эозинофилия, васкулит, узловатая эритема, мультиформная экссудативная эритема (в т. ч. синдром Стивенса-Джонсона), токсический эпидермальный некролиз (синдром Лайелла), анафилактические реакции, анафилактический шок. Со стороны лабораторных показателей: гипопротромбинемия, повышение активности амилазы, "печеночных" трансаминаз, щелочной фосфатазы, гиперкреатининемия, гипербилирубинемия, гипергликемия. Прочие: астения, повышенное потоотделение, суперинфекции (кандидоз,псевдомембранозный колит), "приливы" крови к коже лица. Передозировка: Не существует специфического антидота, поэтому терапия при передозировке препаратом Цифран® СТ должна быть симптоматической и включать следующие мероприятия:вызвать рвоту или провести промывание желудка:проводить меры по адекватной гидратации организма (инфузионная терапия):поддерживающая терапия.С помощью гемо- или перитонеального диализа выведение ципрофлоксацина незначительно (около 10%), но тинидазол может быть полностью выведен из организма. Взаимодействие с другими ЛС: Тинидазол. Усиливает эффект непрямых антикоагулянтов (для уменьшения риска развития кровотечений дозу уменьшают на 50%) и действие этанола (дисульфирамоподобные реакции). Не рекомендуется назначать с этионамидом. Фенобарбитал ускоряет метаболизм. Совместим с сульфаниламидами и антибиотиками (аминогликозиды, эритромицин, рифампицин, цефалоспорины). Ципрофлоксацин. Вследствие снижения активности процессов микросомального окисления в гепатоцитах ципрофлоксацин повышает концентрацию и удлиняет период полувыведения теофиллина (и других ксантинов, например, кофеина), пероральных гипогликемических лекарственных средств, непрямых антикоагулянтов, способствует снижению протромбинового индекса. При сочетании ципрофлоксацина с другими противомикробными лекарственными препаратами (бета-лактамные антибиотики, аминогликозиды, клиндамицин, метронидазол) обычно наблюдается синергизм. Ципрофлоксацин усиливает нефротоксическое действие циклоспорина, при этом отмечается увеличение сывороточного креатинина, вследствие чего необходим контроль этого показателя у пациентов 2 раза в неделю. Пероральный прием ципрофлоксацина совместно с железосодержащими лекарственными средствами, сукральфатом или антацидными лекарственными средствами, содержащими ионы магния, кальция, алюминия, приводит к снижению всасывания ципрофлоксацина, поэтому его следует назначать за 1-2 часа до или через 4 часа после приема вышеуказанных лекарственных средств. Нестероидные противовоспалительные препараты в сочетании с ципрофлоксацином повышают риск развития судорог (за исключением ацетилсалициловой кислоты). Диданозин снижает всасывание ципрофлоксацина вследствие образования комплексов с содержащимися в диданозине ионами магния и алюминия. Метоклопрамид ускоряет абсорбцию ципрофлоксацина, что приводит к уменьшению времени достижения его максимальной концентрации (Стах). Совместное назначение урикозурических лекарственных средств приводит к замедлению выведения (до 50%) и повышению плазменной концентрации ципрофлоксацина. При совместном приеме с тизанидином Стах тизанидина в крови увеличивается в 7 раз (от 4 до 21 раза), вследствие чего развиваются такие побочные эффекты тизанидина, как выраженное снижение артериального давления и сонливость. При одновременном применении с препаратами, удлиняющими интервал QT (антиаритмические средства IA и III классов), возможно удлинение интервала QT на электрокардиограмме. При одновременном применении ципрофлоксацина и омепразола может отмечаться незначительное снижение Стах препарата в плазме и уменьшение площади под кривой "концентрация - время" (AUC). Одновременное применение пробенецида и ципрофлоксацина повышает концентрацию ципрофлоксацина в плазме крови (пробенецид замедляет скорость выведения ципрофлоксацина почками). При одновременном применении с ципрофлоксацином может замедляться почечный метаболизм метотрексата, что может сопровождаться повышением концентрации метотрексата в плазме крови (увеличивается вероятность развития побочных явлений метотрексата). Одновременное применение дулоксетина и мощных ингибиторов изофермента CYP4501A2 (таких как флувоксамин) может привести к увеличению AUC и Сmах дулоксетина. Несмотря на отсутствие клинических данных о возможном взаимодействии с ципрофлоксацином, можно предвидеть вероятность подобного взаимодействия при одновременном применении ципрофлоксацина и дулоксетина. Одновременное применение ропинирола и ципрофлоксацина, умеренного ингибитора изофермента CYP4501A2, приводит к увеличению Сmах и AUC ропинирола на 60% и 84% соответственно. Следует контролировать побочные эффекты ропинирола во время его совместного применения с ципрофлоксацином и в течение короткого времени после завершения комбинированной терапии. При одновременном применении клозапина и ципрофлоксацина в дозе 250 мг в течение 7 дней возможно увеличение сывороточных концентраций клозапина и N - десметилклозапина на 29% и 31% соответственно. Необходима коррекция режима дозирования клозапина во время его совместного применения с ципрофлоксацином и в течение короткого времени после завершения комбинированной терапии. При одновременном применении ципрофлоксацина в дозе 500 мг и силденафила в дозе 50 мг отмечалось увеличение Сmах и AUC силденафила в 2 раза (применение данной комбинации возможно только после оценки соотношения пользы и риска терапии). Одновременное применение лидокаина и ципрофлоксацина приводит к снижению клиренса лидокаина на 22% при его внутривенном введении. Фармакологическое действие и фармакокинетика Фармакодинамика. Цифран® СТ - комбинированный препарат, активными веществами которого являются тинидазол и ципрофлоксацин, предназначенный для терапии инфекций, вызванных анаэробными и аэробными микроорганизмами. Тинидазол обладает противопротозойным и противомикробным действием. Механизм действия связан с угнетением синтеза и нарушением структуры ДНК-чувствительных микроорганизмов. Тинидазол эффективен в отношении простейших (Trichomonas vaginalis, Entamoeba histolytica, Lamblia spp.) и анаэробных микроорганизмов (Clostridium difficile, Clostridium perfringens, Bacteroides fragilis, Peptococcus, Fusobacterium spp, Gardnerella vaginalis, Bacteroides melaninogenicus, Eubacterium spp. и Peptostreptococcus anaerobius). Ципрофлоксацин - антибиотик широкого спектра действия из группы фторхинолонов. Ингибирует фермент ДНК-гиразу бактерий, вследствие чего нарушаются репликация ДНК и синтез клеточных белков бактерий. Активен в отношении большинства аэробных грамположительных и грамотрицательных микроорганизмов, таких как E.coli, Klebsiella spp, S.typhi и другие штаммы Salmonella, Proteus mirabilis, Proteus vulgaris, Yersinia enterocolitica, Pseudomonas aeruginosa, Shigella flexneri, Shigella sonnei, Haemophilus ducreyi, Haemophilus influenzae, Neisseria gonorrhoeae, Moraxella catarrhalis, Vibrio cholerae, Staphylococcus aureus (включая метициллин устойчивые штаммы), Staphylococcus epidermidis, Streptococcus pyogenes, Streptococcus pneumoniae, Chlamydia trachomatis, Chlamydia pneumonia, Mycoplasma pneumonia, Mycoplasma hominis, Legionella pneumophila и Mycobacterium tuberculosis. Фармакокинетика: Как ципрофлоксацин, так и тинидазол хорошо абсорбируются в желудочно-кишечном тракте. Пиковые концентрации каждого компонента достигаются в течение 1 - 2 часов. Биодоступность тинидазола - 100%, а связывание с белками плазмы крови - 12%. Период полувыведения около 12-14 часов. Тинидазол быстро проникает в ткани организма, достигая там высоких концентраций, проникает в цереброспинальную жидкость в концентрации равной его концентрации в плазме и подвергается обратному всасыванию в почечных канальцах. Тинидазол экскретируется в желчь в концентрациях несколько ниже 50% его концентрации в сыворотке крови. Около 25% от принятой дозы выводится в неизмененном виде почками. Метаболиты составляют 12% от введенной дозы и выводятся также почками. Наряду с этим наблюдается незначительное выведение тинидазола через желудочно-кишечный тракт. Ципрофлоксацин хорошо абсорбируется после применения внутрь. Биодоступность ципрофлоксацина около 70%. При совместном применении с пищей абсорбция ципрофлоксацина замедляется. 20-40% ципрофлоксацина связывается с белками плазмы. Ципрофлоксацин хорошо проникает в жидкостные среды и ткани организма: легкие,кожу, жировую, мышечную и хрящевую ткани, а также в костную ткань и органы мочеполовой системы, включая предстательную железу. Ципрофлоксацин обнаруживается в высоких концентрациях в слюне, слизи носовой полости и бронхах, лимфе, перитонеальной жидкости, желчи и семенной жидкости. Частично ципрофлоксацин метаболизируется печенью. Около 50% от принятой дозы выводится в неизмененном виде почками. 15% от принятой дозы выводится почками в виде активных метаболитов, таких как оксоципрофлоксацин. Остальная часть дозы выводится с желчью, частично всасываясь повторно. Около 15 - 30% ципрофлоксацина выводится через желудочно-кишечный тракт. Период полувыведения около 3,5 - 4,5 часов. Период полувыведения может удлиняться при выраженной почечной недостаточности и у пожилых пациентов. Особые указания Следует учитывать возможность возникновения перекрестных аллергических реакций на тинидазол и ципрофлоксацин у пациентов с гиперчувствительностью к другим производным имидазола и фторхинолона соответственно.В период лечения препаратом Цифран* СТ следует избегать длительного воздействия ультрафиолетового излучения, в т.ч. длительного пребывания под прямыми солнечными лучами, во избежание реакций фототоксичности. При совместном применении тинидазола с этанолом могут возникать болезненные спазмы в животе, тошнота и рвота. Совместное применение Цифран СТ и этанола противопоказано. Во избежание развития кристаллурии недопустимо превышение рекомендованнойсуточной дозы, необходимо также достаточное потребление жидкости и поддержание кислой реакции мочи. Прием препарата вызывает темное окрашивание мочи (не имеет клинического значения). Больным с эпилепсией, приступами судорог в анамнезе, сосудистыми заболеваниями и органическими поражениями мозга, в связи с угрозой развития побочных реакций со стороны центральной нервной системы, препарат следует назначать только по "жизненным" показаниям. При возникновении во время или после лечения тяжелой и длительной диареи следует исключить диагноз псевдомембранозного колита, который требует немедленной отмены препарата и назначения соответствующего лечения. При появлении болей в сухожилиях или при проявлении первых признаков тендовагинита лечение следует прекратить.В процессе лечения следует контролировать картину периферической крови. Влияние на способность управлять транспортными средствами: Следует соблюдать осторожность при вождении автомобиля и занятиях другими потенциально опасными видами деятельности, требующими повышенного внимания и быстроты психомоторных реакций. Условия хранения и отпуска из аптек Условия хранения:Хранить в сухом месте при температуре не выше 25°С. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Цифран® СТ Международное непатентованное название:Тинидазол + Ципрофлоксацин. Форма выпуска:таблетки покрытые пленочной оболочкой. Состав:Каждая таблетка содержит:Активные вещества:тинидазол 600 мгципрофлоксацина гидрохлорид 610,66 мг,эквивалентный ципрофлоксацину 500 мг. Вспомогательные вещества: целлюлоза микрокристаллическая* - 83,68 мг, кремния диоксид коллоидный - 28,00 мг, магния стеарат - 9,334 мг, карбоксиметилкрахмал натрия - 56,00 мг, натрия лаурилсульфат - 10,00 мг, тальк очищенный - 2,334 мг. Оболочка таблетки: опадрай желтый 31F52949 - 38,50 мг, вода очищенная* - q.s. Опадрай желтый 31F52949: НРМС 2910/Гипромеллоза 15 ср - 36,00% масса/масса, лактозы моногидрат - 28,00% масса/масса, титана диоксид - 20,962% масса/масса, макрогол 4000 - 10,00% масса/масса, краситель железа оксид желтый - 5,038% масса/масса. количество корректируется, основываясь на фактическом количестве ципрофлоксацина гидрохлорида и тинидазола, для поддержания постоянной массы таблетки. испаряется в процессе производства. АТХ: Регистрация: Лекарственное средство П N015922/01 Фармгруппа: противомикробное средство комбинированное. Дата регистрации: 23.07.2008. Окончание регстрации: . Описание:двояковыпуклые таблетки овальной формы, желтого цвета, с риской на одной стороне, покрытые пленочной оболочкой. Вид таблеток на изломе: однородная прессованная масса от белого до почти белого цвета Упаковка:Таблетки, покрытые пленочной оболочкой, 600 мг + 500 мг.10 таблеток в блистере из алюминиевой фольги и ПВХ.1 или 2 блистера с инструкцией по применению в картонной пачке. 10 таблеток в блистере из алюминиевой фольги и ПВХ.1 или 2 блистера с инструкцией по применению в картонной пачке. Срок годности:2 года. Не использовать после истечения срока годности. Владелец рег.удостоверения:Ранбакси Лабораториз Лимитед Производитель:RANBAXY LABORATORIES, Ltd. Представительство:РАНБАКСИ ЛАБОРАТОРИЗ ЛИМИТЕД

Модель:
RUR 766
Показания Сахарный диабет 2 типа (в сочетании с диетотерапией и физическими упражнениями)- в качестве монотерапии в случае неэффективности диетотерапии и физических упражнений у пациентов с противопоказанием к применению метформина или в случае неэффективности метформина- в комбинации с метформином в качестве начальной медикаментозной терапии при недостаточной эффективности диетотерапии и физических упражнений- в составе двухкомпонентной комбинированной терапии с метформином, производным сульфонилмочевины, тиазолидиндионом или с инсулином в случае неэффективности диетотерапии, физических упражнений и монотерапии этими препаратами- в составе тройной комбинированной терапии: в комбинации с производными сульфонилмочевины и метформином, у пациентов, ранее получавших терапию производными сульфонилмочевины и метформином на фоне диетотерапии и физических упражнений и не достигших адекватного контроля гликемии- в составе тройной комбинированной терапии: в комбинации с инсулином и метформином, у пациентов, ранее получавших инсулин и метформин на фоне диетотерапии и физических упражнений и не достигших адекватного контроля гликемии. Противопоказания Противопоказания - Повышенная чувствительность к вилдаглиптину и любым другим компонентам препарата- наследственная непереносимость галактозы, недостаточность лактазы, глюкозо-галактозная мальабсорбция- беременность, грудное вскармливание (в связи с недостатком соответствующих данных)- сахарный диабет 1 типа- острый или хронический метаболический ацидоз (включая диабетический кетоацидоз в сочетании с комой или без таковой). Диабетический кетоацидоз должен корректироваться инсулинотерапией. Лактоацидоз (в том числе и в анамнезе)- нарушения функции печени, включая пациентов с повышенной активностью "печеночных" ферментов (аланинаминотрансферазы (АЛТ) или аспартатаминотрансферазы (ACT) в 3 и более раз выше верхней границы нормы, (3хВГН)- хроническая сердечная недостаточность (ХСН) IV функционального класса (ФК) по функциональной классификации Нью-Йоркской кардиологической ассоциации (NYHA) (ввиду отсутствия данных клинических исследований о применении вилдаглиптина у этой группы пациентов): - детский возраст до 18 лет (эффективность и безопасность применения препарата не установлены). С осторожностью: Рекомендуется с осторожностью применять препарат Галвус у пациентов с острым панкреатитом в анамнезе. Поскольку опыт применения препарата Галвус у пациентов с терминальной стадией ХБП, находящихся на гемодиализе или проходящих процедуру гемодиализа, ограничен, препарат рекомендуется применять с осторожностью у данной категории пациентов. Поскольку данные о применении вилдаглиптина у пациентов с ХСН III ФК по классификации NYHA ограничены и не позволяют сделать окончательный вывод, рекомендуется с осторожностью применять препарат Галвус у пациентов данной категории. Беременность Достаточных данных по применению препарата Галвус у беременных нет, в связи с чем препарат противопоказан во время беременности. В доклинических исследованиях была выявлена репродуктивная токсичность при применении в высоких дозах, потенциальный риск для человека неизвестен. Препарат Галвус противопоказан в период грудного вскармливания, поскольку неизвестно, проникает ли вилдаглиптин в грудное молоко у человека. Применение и дозы Дозу препарата Галвус следует подбирать индивидуально в зависимости от эффективности и переносимости. Рекомендуемая доза препарата Галвус 50 мг 1 или 2 раза в день. Максимальная суточная доза препарата составляет 100 мг. Дозу 50 мг/сут следует принимать 1 раз в день утром, дозу 100 мг/сут следует делить на 2 приема - по 50 мг утром и вечером. В случае пропуска приема препарата следует принять пропущенную дозу как можно скорее. При этом следует избегать принятия удвоенной дозы в один день. Препарат Галвус принимают внутрь независимо от приема пищи. Рекомендуемая доза препарата в монотерапии или в составе комбинированной терапии с метформином, тиазолидиндионом или инсулином (в комбинации с метформином или без метформина), составляет 50 мг или 100 мг в сутки. Рекомендуемая доза препарата Галвус в составе двойной комбинированной терапии с препаратами сульфонилмочевины составляет 50 мг 1 раз в сутки утром. В этой популяции пациентов эффективность препарата Галвус в дозе 100 мг в сутки была сходной с таковой в дозе 50 мг в сутки. Рекомендованная доза препарата Галвус в составе тройной комбинированной терапии (вилдаглиптин + производные сульфонилмочевины + метформин) составляет 100 мг в сутки. Если цели гликемического контроля не достигнуты на фоне применения максимальной суточной дозы 100 мг, следует рассмотреть возможность добавления к терапии препаратом Галвус других гипогликемических препаратов, таких, как метформин, производные сульфонилмочевины, тиазолидиндион или инсулин. Пациенты с нарушениями функции почекУ пациентов с нарушением функции почек легкой степени (СКФ 60 мл/мин/1,73 м 2) и средней степени с СКФ 50-60 мл/мин/1,73 м 2 не требуется коррекции режима дозирования препарата. У пациентов с нарушением функции почек средней степени с СКФ 30- 50 мл/мин/1,73 м 2 и тяжелой степени (СКФ <:30 мл/мин/1,73 м 2), включая терминальную стадию ХБП у пациентов, находящихся на гемодиализе или проходящих процедуру гемодиализа, препарат следует применять в дозе 50 мг 1 раз в сутки. Пациенты в возрасте 65 летУ пациентов пожилого возраста не требуется коррекции режима дозирования препарата Галвус. Пациенты в возрасте 18 лет Поскольку опыта применения препарата Галвус у детей и подростков младше 18 лет нет, не рекомендуется применять препарат у пациентов данной категории. Побочные эффекты и передозировка Побочные эффекты: При применении препарата Галвус в монотерапии или в комбинации с другими препаратами большинство нежелательных реакций были слабо выражены, имели временный характер и не требовали отмены терапии. Корреляции между частотой нежелательных явлений (НЯ) и возрастом, полом, этнической принадлежностью, продолжительностью применения или режимом дозирования не выявлено. Частота развития ангионевротического отека на фоне терапии препаратом Галвус составляла 1/10000, <:1/1000 (градация "редко") и была сходной с таковой в контрольной группе. Наиболее часто случаи ангионевротического отека отмечались при применении препарата в комбинации с ингибиторами ангиотензинпревращающего фермента. В большинстве случаев ангионевротический отек был средней степени тяжести и разрешался самостоятельно в ходе продолжения терапии вилдаглиптином. На фоне терапии препаратом Галвус редко отмечались нарушения функции печени (включая гепатит) бессимптомного течения. В большинстве случаев данные нарушения и отклонения показателей функции печени от нормы разрешились самостоятельно без осложнений после прекращения терапии препаратом. При применении препарата Галвус в дозе 50 мг 1 или 2 раза в сутки частота увеличения активности "печеночных" ферментов (АЛТ или ACT 3 х ВГН) составляла 0,2% или 0,3% соответственно (по сравнению с 0,2% в контрольной группе). Увеличение активности "печеночных" ферментов в большинстве случаев было бессимптомным, не прогрессировало и не сопровождалось холестазом или желтухой.НЯ сгруппированы в соответствии с классификацией органов и систем органов MedDRA. В пределах каждой группы органов и систем органов НЯ перечислены в порядке уменьшения частоты встречаемости. В пределах каждой группы частоты встречаемости НЯ указаны в порядке уменьшения тяжести. Для оценки частоты встречаемости нежелательных явлений использовались следующие критерии: очень часто ( 1/10), часто ( 1/100, <:1/10), нечасто ( 1/1 000, <:1/100), редко ( 1/10 000, <:1/1 000), очень редко (<:1/10 000), отдельные сообщения (частота неизвестна). При применении препарата Галвус в монотерапии. При применении препарата Галвус в дозе 50 мг 1 или 2 раза в сутки частота отмены терапии в связи с развитием нежелательных реакций (0,2% или 0,1% соответственно) была не выше таковой в группе плацебо (0,6%) или препарата сравнения (0,5%). На фоне монотерапии препаратом Галвус в дозе 50 мг 1 или 2 раза в сутки частота развития гипогликемии без увеличения степени тяжести состояния составляла 0,5% (2 пациента из 409) и 0,3% (4 из 1082) соответственно, что сопоставимо с препаратом сравнения и плацебо (0,2%). Инфекционные и паразитарные заболевания: очень редко - инфекции верхних дыхательных путей, назофарингит. Нарушения со стороны нервной системы: часто - головокружение: нечасто - головная боль. Нарушения со стороны желудочно-кишечного тракта: нечасто - запор. Нарушения со стороны сосудов: нечасто - периферические отеки. Долгосрочные клинические исследования продолжительностью до 2 лет не выявили каких-либо дополнительных отклонений профиля безопасности или непредвиденных рисков при применении вилдаглиптина в монотерапии. При применении препарата Галвус в дозе 50 мг 1 или 2 раза в сутки в комбинации с метформином. При применении препарата Галвус в дозе 50 мг/сут в комбинации с метформином частота отмены терапии в связи с развитием нежелательных реакций составляла 0,4% (в группах вилдаглиптин (50 мг 2 раза в сутки) + метформин и плацебо + метформин случаев отмены терапии в связи с развитием нежелательных реакций не отмечалось). При применении препарата Галвус в дозе 50 мг 1 или 2 раза в сутки в комбинации с метформином гипогликемия отмечалась в 0,9% и 0,5% случаев соответственно (в группе плацебо + метформин - 0,4%). В группе применения препарата Галвус не наблюдалось развития гипогликемии тяжелой степени. Комбинированная терапия вилдаглиптин + метформин не влияла на массу тела пациентов. Нарушения со стороны нервной системы: часто - тремор, головокружение, головная боль. Нарушения со стороны желудочно-кишечного тракта: часто - тошнота. Долгосрочные клинические исследования продолжительностью до 2 лет не выявили каких-либо дополнительных отклонений профиля безопасности или непредвиденных рисков при применении вилдаглиптина в комбинации с метформином. Изучение применения комбинации вилдаглиптина и метформина в качестве стартовой терапии при сахарном диабете 2 типа не выявило отклонений профиля безопасности или непредвиденных рисков. При применении препарата Галвус в дозе 50 мг/сут в комбинации с производными сульфонилмочевины. При применении препарата Галвус в дозе 50 мг/сут в комбинации с глимепиридом частота отмены терапии в связи с развитием нежелательных реакций составляла 0,6% (по сравнению с 0% в группе глимепирид + плацебо). Частота развития гипогликемии у пациентов, получавших препарат Галвус в дозе 50 мг/сут вместе с глимепиридом, составила 1,2% (по сравнению с 0,6% в группе плацебо + глимепирид). В группе применения препарата Галвус не наблюдалось развития гипогликемии тяжелой степени. При применении препарата Галвус в рекомендованной дозе (50 мг/сут) в комбинации с глимепиридом не отмечалось увеличения массы тела. Инфекционные и паразитарные заболевания: очень редко - назофарингит. Нарушения со стороны желудочно-кишечного тракта: нечасто - запор. Нарушения со стороны нервной системы: часто - тремор, головокружение, головная боль, астения. При применении препарата Галвус в дозе 50 мг 1 или 2 раза в сутки в комбинации с производными тиазолидиндиона. При применении препарата Галвус в дозе 50 мг/сут в комбинации с пиоглитазоном частота отмены терапии в связи с развитием нежелательных реакций составляла 0,7% (в группах вилдаглиптин 100 мг/сут + пиоглитазон и плацебо + пиоглитазон случаев отмены терапии в связи с развитием нежелательных реакций не отмечалось). При применении препарата Галвус в дозе 50 мг/сут в комбинации с пиоглитазоном в дозе 45 мг развития гипогликемии не отмечалось: в группе вилдаглиптин (в дозе 50 мг 2 раза в сутки) + пиоглитазон (в дозе 45 мг) отмечалось развитие гипогликемии в 0,6% случаев, а у пациентов, получавших плацебо + пиоглитазон в дозе 45 мг, - в 1,9% случаев. В группе применения препарата Галвус не наблюдалось развития гипогликемии тяжелой степени. Среднее увеличение массы тела по сравнению с плацебо у пациентов, получавших препарат Галвус в дозе 50 мг 1 или 2 раза в сутки вместе с пиоглитазоном, составляло +0,1 кг или +1,3 кг соответственно. При добавлении препарата Галвус в дозе 50 мг 1 или 2 раза в сутки к пиоглитазону в дозе 45 мг/сут частота развития периферических отеков составляла 8,2% и 7% соответственно (по сравнению с 2,5% на фоне монотерапии пиоглитазоном). Однако при начальной комбинированной терапии вилдаглиптином в дозе 50 мг 1 или 2 раза в сутки вместе с пиоглитазоном в дозе 45 мг/сут развитие периферических отеков наблюдалось у 3,5% или 6,1% пациентов соответственно (по сравнению с 9,3% на фоне монотерапии пиоглитазоном в дозе 30 мг/сут). Нарушения со стороны сосудов: часто - периферические отеки. Нарушения со стороны обмена веществ и питания: часто - увеличение массы тела. При применении препарата Галвус в дозе 50 мг 2 раза в сутки в комбинации с инсулином (с метформином или без него)При применении препарата в комбинации с инсулином (в комбинации с метформином или без метформина) частота отмены терапии вследствие развития побочных эффектов была равна 0,3%, в группе терапии вилдаглиптином, в группе плацебо случаев отмены терапии не было. При применении препарата в комбинации с инсулином (в комбинации с метформином или без метформина) не отмечалось увеличения риска развития гипогликемии по сравнению с комбинацией плацебо + инсулин (14% в группе вилдаглиптина и 16,4% в группе плацебо). У 2 пациентов в группе вилдаглиптина и у 6 пациентов в группе плацебо развилась гипогликемия тяжелой степени. На момент завершения исследования препарат не оказывал влияния на среднюю массу тела (масса тела увеличена на +0,6 кг по сравнению с исходной в группе вилдаглиптина, а в группе плацебо осталась неизменной). Нарушения со стороны нервной системы: часто - головная боль, неизвестно - астения. Нарушения со стороны желудочно-кишечного тракта: часто - тошнота, гастроэзофагеальный рефлюкс: нечасто - диарея, метеоризм. Общие расстройства и нарушения в месте введения: часто - озноб. Нарушения со стороны обмена веществ и питания: часто - гипогликемия. При применении препарата Галвус в дозе 50 мг два раза в день в комбинации с препаратами сульфонилмочевины и метформином. Случаев отмены препарата, связанных с НЯ в группе комбинированной терапии вилдаглиптином, метформином и глимепиридом, отмечено не было. В группе комбинированной терапии плацебо, метформином и глимепиридом частота НЯ составила 0,6%. Гипогликемия отмечалась часто в обеих группах (5,1% в группе комбинированной терапии вилдаглиптином, метформином и глимепиридом и 1,9% в группе комбинированной терапии плацебо, метформином и глимепиридом). В группе вилдаглиптина отмечен один эпизод гипогликемии тяжелой степени. На момент завершения исследования значимого влияния на массу тела выявлено не было (+0,6 кг в группе вилдаглиптина и -0,1 кг в группе плацебо). Нарушения со стороны нервной системы: часто - головокружение, тремор, астения. Нарушения со стороны обмена веществ и питания: часто - гипогликемия. Нарушения со стороны кожи и подкожных тканей: часто - гипергидроз. Пострегистрационные исследования. Во время проведения пострегистрационных исследований были выявлены следующие побочные реакции (поскольку сообщения получены в добровольном порядке от популяции неопределенного размера, достоверно определить частоту развития данных НЯ не представляется возможным, в связи с чем они классифицированы как частота неизвестна): гепатит (обратим при прекращении терапии), крапивница, панкреатит, буллезное и эксфолиативное поражение кожи, артралгия, в редких случаях выраженная, миалгия, повышение активности "печеночных" ферментов. Если любые из указанных в инструкции побочных эффектов усугубляются, или Вы заметили любые другие побочные эффекты, не указанные в инструкции, сообщите об этом врачу. Передозировка: Вилдаглиптин хорошо переносится при применении в дозе до 200 мг/сут. При применении препарата в дозе 400 мг/сут может наблюдаться боль в мышцах, редко - легкие и транзиторные парестезии, лихорадка, отеки и транзиторное повышение активности липазы (выше ВГН в 2 раза). При увеличении дозы вилдаглиптина до 600 мг/сут возможно развитие отеков конечностей, сопровождающихся парестезиями и повышением активности креатинфосфокиназы, С-реактивного белка и миоглобина, активности ACT. Все симптомы передозировки и изменения лабораторных показателей обратимы после прекращения применения препарата. Выведение препарата из организма с помощью диализа маловероятно. Однако основной гидролизный метаболит вилдаглиптина (LAY151) может быть удален из организма путем гемодиализа. Взаимодействие с другими ЛС: Вилдаглиптин обладает низким потенциалом лекарственного взаимодействия. Поскольку вилдаглиптин не является субстратом ферментов цитохрома Р450 (CYP), а также не ингибирует и не индуцирует эти ферменты, взаимодействие вилдаглиптина с лекарственными препаратами, которые являются субстратами, ингибиторами или индукторами Р450 (CYP), маловероятно. При одновременном применении вилдаглиптин также не влияет на скорость метаболизма препаратов, являющихся субстратами ферментов: CYP1A2, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 и CYP3A4/5. Клинически значимого взаимодействия вилдаглиптина с препаратами, наиболее часто используемыми при лечении СД 2 типа (глибенкламидом, пиоглитазоном, метформином) или обладающими узким терапевтическим диапазоном (амлодипином, дигоксином, рамиприлом, симвастатином, валсартаном, варфарином) не установлено. Тиазиды, глюкокортикостероиды, препараты гормонов щитовидной железы, симпатомиметики могут снижать гипогликемическое действие вилдаглиптина, как и других пероральных противодиабетических препаратов. Частота развития ангионевротического отека была выше при одновременном применении вилдаглиптина с ингибиторами ангиотензинпревращающего фермента, при этом была сходной с таковой в контрольной группе. В большинстве случаев ангионевротический отек был средней степени тяжести и разрешался самостоятельно в ходе продолжения терапии вилдаглиптином. Фармакологическое действие и фармакокинетика Механизм действия. Вилдаглиптин - представитель класса стимуляторов островкового аппарата поджелудочной железы, селективно ингибирует фермент дипептидилпептидазу-4 (ДПП-4). Быстрое и полное ингибирование активности ДПП-4 (>:90%) вызывает повышение как базальной, так и стимулированной приемом пищи секреции глюкагоноподобного пептида 1 типа (ГПП-1) и глюкозозависимого инсулинотропного полипептида (ГИП) из кишечника в системный кровоток в течение всего дня. Повышая концентрацию ГПП-1 и ГИП, вилдаглиптин вызывает повышение чувствительности β-клеток поджелудочной железы к глюкозе, что приводит к улучшению глюкозозависимой секреции инсулина. Фармакодинамика. При применении вилдаглиптина в дозе 50-100 мг в сутки у пациентов с сахарным диабетом 2 типа (СД 2 типа) отмечается улучшение функции β-клеток поджелудочной железы. Степень улучшения функции β-клеток зависит от степени их исходного повреждения: так у лиц без СД (с нормальной концентрацией глюкозы в плазме крови) вилдаглиптин не стимулирует секрецию инсулина и не снижает концентрацию глюкозы. Повышая концентрацию эндогенного ГПП-1, вилдаглиптин увеличивает чувствительность α-клеток к глюкозе, что приводит к улучшению глюкозозависимой регуляции секреции глюкагона. Снижение повышенной концентрации глюкагона во время еды, в свою очередь, вызывает уменьшение инсулинорезистентности. Увеличение соотношения инсулин/глюкагон на фоне гипергликемии, обусловленное повышением концентрации ГПП-1 и ГИП, вызывает уменьшение продукции глюкозы печенью как во время, так и после приема пищи, что приводит к снижению концентрации глюкозы в плазме крови. Кроме того, на фоне применения вилдаглиптина отмечается снижение концентрации липидов в плазме крови после приема пищи, однако этот эффект не связан с его действием на ГПП-1 или ГИП и улучшением функции островковых клеток поджелудочной железы. Известно, что повышение концентрации ГПП-1 может приводить к замедлению опорожнения желудка, однако на фоне применения вилдаглиптина подобного эффекта не наблюдается. При применении вилдаглиптина у 5795 пациентов с СД 2 типа в течение 52 недель в монотерапии или в комбинации с метформином, производными сульфонилмочевины, тиазолидиндионом, или инсулином отмечалось достоверное длительное снижение концентрации гликированного гемоглобина (Hb. Alc) и глюкозы крови натощак. При применении комбинации вилдаглиптина и метформина в качестве начальной терапии у пациентов с сахарным диабетом 2 типа в течение 24 недель отмечалось дозозависимое снижение концентрации HbA1c в сравнении с монотерапией данными препаратами. Случаи развития гипогликемии были минимальны в обеих группах терапии. При применении вилдаглиптина в дозе 50 мг 1 раз в сутки в течение 6 месяцев у пациентов с СД 2 типа с нарушением функции почек средней (скорость клубочковой фильтрации (СКФ) 30, <:50 мл/мин/1,73 м 2) или тяжелой (СКФ <:30 мл/мин/1,73 м 2) степени отмечалось клинически значимое снижение концентрации HbA1c по сравнению с плацебо. При применении вилдаглиптина в дозе 50 мг 2 раза в сутки в комбинации с/без метформина и инсулином (средняя доза 41 ЕД/сут) было продемонстрировано снижение показателя HbA1c на 0,77% от исходного среднего значения 8,8% со статистически достоверной разницей с плацебо 0,72%. Частота гипогликемии в группе вилдаглиптина сравнима с таковой в группе плацебо. При применении вилдаглиптина в дозе 50 мг 2 раза в сутки в комбинации с метформипом ( 1500 мг/сут) и глимепиридом ( 4 мг/сут) было показано статистически значимое снижение уровня HbA1c на 0,76% от исходного среднего значения 8,8%. Фармакокинетика: Всасывание. При приеме внутрь натощак вилдаглиптин быстро всасывается, а его максимальная концентрация в плазме крови (Сmах) достигается через 1,75 часа после приема. При одновременном приеме с пищей скорость абсорбции вилдаглиптина снижается незначительно: отмечается уменьшение Сmах на 19% и увеличение времени ее достижения до 2,5 часов. Однако прием пищи не оказывает влияния на степень абсорбции и площадь под кривой "концентрация-время" (AUC). Вилдаглиптин быстро всасывается, а его абсолютная биодоступность после приема внутрь составляет 85%. Сmах и AUC в терапевтическом диапазоне доз увеличиваются примерно пропорционально дозе. Распределение. Степень связывания вилдаглиптина с белками плазмы крови низкая (9,3%). Вилдаглиптин распределяется равномерно между плазмой крови и эритроцитами. Распределение вилдаглиптина происходит, предположительно, экстраваскулярно, объем распределения в равновесном состоянии после внутривенного введения (Vss) составляет 71 л. Метаболизм. Основным путем выведения вилдаглиптина является биотрансформация. В организме человека 69% дозы препарата подвергается биотрансформации. Основной метаболит - LAY151 (57% дозы) фармакологически неактивен и является продуктом гидролиза цианокомпонента. Около 4% дозы препарата подвергаются амидному гидролизу.В доклинических исследованиях отмечается положительное влияние ДПП-4 на гидролиз вилдаглиптина. Вилдаглиптин метаболизируется без участия изоферментов цитохрома Р450. Вилдаглиптин не является субстратом изоферментов Р450 (CYP), не ингибирует и не индуцирует изоферменты цитохрома Р450. Выведение. После приема препарата внутрь около 85% дозы выводится почками и 15% - через кишечник. Почечная экскреция неизмененного вилдаглиптина составляет 23%. При внутривенном введении средний период полувыведения достигает 2 часов, общий плазменный клиренс и почечный клиренс вилдаглиптина составляют 41 л/ч и 13 л/ч соответственно. Период полувыведения (Т1/2) после приема внутрь составляет около 3 часов, независимо от дозы. Фармакокинетика в особых случаях. Пол, индекс массы тела и этническая принадлежность не оказывают влияния на фармакокинетику вилдаглиптина. Пациенты с нарушением функции печениУ пациентов с нарушением функции печени легкой и средней степеней тяжести (6-9 баллов по шкале Чайлд-Пью) после однократного применения препарата отмечается снижение биодоступности вилдаглиптина на 20% и 8% соответственно. У пациентов с нарушением функции печени тяжелой степени (10-12 баллов по шкале Чайлд-Пью) биодоступность вилдаглиптина повышается на 22%. Увеличение или уменьшение максимальной биодоступности вилдаглиптина, не превышающее 30%, не является клинически значимым. Корреляции между степенью тяжести нарушений функции печени и биодоступностью препарата не выявлено. Пациенты с нарушением функции почекУ пациентов с нарушением функции почек легкой, средней или тяжелой степени AUC вилдаглиптина увеличивалась по сравнению со здоровыми добровольцами в 1,4, 1,7 и 2 раза соответственно. AUC метаболита LAY151 увеличивалась в 1,6, 3,2, и 7,3 раза, а метаболита BQS867 - в 1,4, 2,7, и 7,3 раза у пациентов с нарушением функции почек легкой, средней и тяжелой степеней соответственно. Ограниченные данные у пациентов с терминальной стадией хронической болезни почек (ХБП) указывают на то, что показатели данной группы схожи с таковыми у пациентов с нарушением функции почек тяжелой степени. Концентрация метаболита LAY151 у пациентов с терминальной стадией ХБП увеличивалась в 2-3 раза по сравнению с концентрацией у пациентов с нарушением функции почек тяжелой степени. При применении препарата у пациентов с нарушением функции почек может потребоваться коррекция дозы. Выведение вилдаглиптина при гемодиализе ограничено (через 4 часа после однократного приема составляет 3% при длительности процедуры более 3-4 часов). Применение у пациентов в возрасте 65 лет. Максимальное увеличение биодоступности препарата на 32% (увеличение Сmах на 18%) у пациентов старше 70 лет не является клинически значимым и не влияет на ингибирование ДПП-4. Применение у пациентов в возрасте 18 лет. Фармакокинетические особенности вилдаглиптина у детей и подростков младше 18 лет не установлены. Особые указания В доклинических исследованиях при применении в дозах, в 200 раз превышающих рекомендуемые для человека, препарат не вызывал нарушений фертильности. При необходимости инсулинотерапии препарат Галвус применяют только в комбинации с инсулином. Препарат противопоказан у пациентов с сахарным диабетом 1 типа или для лечения диабетического кетоацидоза. Сердечная недостаточность. Поскольку данные о применении вилдаглиптина у пациентов с ХСН III ФК по классификации NYHA (см. Таблицу 1, приведенную ниже) ограничены и не позволяют сделать окончательный вывод, рекомендуется с осторожностью применять препарат Галвус у пациентов данной категории. Не рекомендуется применение вилдаглиптина у пациентов с ХСН IV ФК по классификации NYHA, ввиду отсутствия данных клинических исследований о применении вилдаглиптина у пациентов этой группы. Таблица 1. Нью-Йоркская классификация функционального состояния пациентов с хронической сердечной недостаточностью (в модификации), NYHA, 1964.ТАБЛИЦЪНарушения функции печени. Поскольку в редких случаях при применении вилдаглиптина отмечалось повышение активности аминотрансфераз (как правило, без клинических проявлений), перед применением препарата Галвус, а также и регулярно в ходе первого года применения препарата (1 раз в 3 месяца), рекомендуется определять биохимические показатели функции печени. При выявлении повышения активности аминотрансфераз следует провести повторное исследование с целью подтверждения результата, а затем регулярно проводить определение биохимических показателей функции печени до их нормализации. Если превышение активности ACT или АЛТ в 3 или более раз выше ВГН подтверждено повторным исследованием, препарат рекомендуется отменить. При развитии желтухи или других признаков нарушения функции печени на фоне применения препарата Галвус терапию препаратом следует немедленно прекратить. После нормализации показателей функции печени лечение препаратом возобновлять нельзя. Гипогликемия. Известно, что препараты сульфонилмочевины могут провоцировать развитие гипогликемии. Существует риск развития гипогликемии при одновременном применении вилдаглиптина с препаратами сульфонилмочевины. При необходимости следует рассмотреть возможность снижения дозы препаратов сульфонилмочевины с целью минимизировать риск развития гипогликемии. Острый панкреатит Применение вилдаглиптина связано с риском развития острого панкреатита. Следует проинформировать пациента о симптомах, характерных для острого панкреатита. При подозрении на острый панкреатит вилдаглиптин следует отменить. Не следует возобновлять терапию вилдаглиптином, если острый панкреатит был подтвержден. У пациентов с острым панкреатитом в анамнезе применять вилдаглиптин следует с осторожностью. Влияние на способность управлять транспортными средствами: Исследования влияния препарата Галвус на способность управлять транспортными средствами или работать с механизмами не проводились. При развитии головокружения на фоне применения препарата пациентам не следует управлять транспортными средствами или работать с механизмами. Условия хранения и отпуска из аптек Условия хранения:В оригинальной упаковке, при температуре не выше 30 °С. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Галвус Международное непатентованное название:Вилдаглиптин. Форма выпуска:таблетки. Состав:1 таблетка содержит: действующее вещество: вилдаглиптин 50,0 мг:вспомогательные вещества: целлюлоза микрокристаллическая - 95,68 мг, лактоза - 47,82 мг, карбоксиметилкрахмал натрия - 4,0 мг, магния стеарат - 2,5 мг. АТХ: Регистрация: Лекарственное средство ЛСР-008119/08 Фармгруппа: Гипогликемическое средство - дипептидилпептидазы-4 ингибитор. Дата регистрации: 14.10.2008 / 14.10.2016. Окончание регстрации: . Описание:От белого до светло-желтого цвета, круглые, гладкие таблетки со скошенными краями, с гравировкой “NVR" на одной стороне и “FB” на другой стороне. Упаковка:Таблетки, 50 мг. По 7 или 14 шт. в блистере. По 2, 4, 8, 12 блистеров вместе с инструкцией по применению в картонной пачке. Срок годности:3 года. Не применять по истечении срока годности. Владелец рег.удостоверения:Новартис Фарма АГ Производитель:NOVARTIS FARMACEUTICA, S.A. : NOVARTIS PHARMA STEIN, AG : ОРТАТ, ЗАО. Представительство:НОВАРТИС ФАРМА ООО
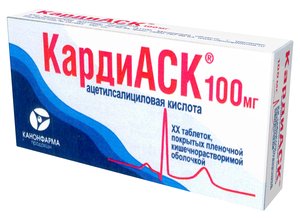
Модель:
RUR 106
Показания Первичная профилактика острого инфаркта миокарда при наличии факторов риска (сахарный диабет, гиперлипидемия, артериальная гипертензия, ожирение, курение, пожилой возраст) и повторного инфаркта миокарда: - Нестабильная стенокардия (включая подозрение на развитие острого инфаркта миокарда) и стабильная стенокардия: - Профилактика инсульта (в том числе у пациентов с преходящим нарушением мозгового кровообращения): - Профилактика преходящего нарушения мозгового кровообращения: - Профилактика тромбоэмболии после операций и инвазивных вмешательств на сосудах (аортокоронарное шунтирование, эндартерэктомия сонных артерий, артериовенозное шунтирование, ангиопластика и стентирование коронарных артерий, ангиопластика сонных артерий): - Профилактика тромбоза глубоких вен и тромбоэмболии легочной артерии и ее ветвей (в том числе, при длительной иммобилизации в результате обширного хирургического вмешательства). Противопоказания Противопоказания - Повышенная чувствительность к АСК, вспомогательным веществам в составе препарата и другим нестероидным противовоспалительным препаратам (НПВП): - Дефицит лактазы, непереносимость лактозы, глюкозо-галактозная мальабсорбция: - Эрозивно-язвенные поражения ЖКТ (в стадии обострения): - Желудочно-кишечное кровотечение: - Геморрагический диатез: - Бронхиальная астма, индуцированная приемом салицилатов и других НПВП: сочетание бронхиальной астмы, рецидивирующего полипоза носа и околоносовых пазух и непереносимости АСК: - Одновременный прием метотрексата в дозе 15 мг в неделю и более: - Беременность (I и III триместр), период лактации: - Возраст до 18 лет: - Выраженная почечная недостаточность (клиренс креатинина (КК) менее 30 мл/мин): - Выраженная печеночная недостаточность (класс В и выше по шкале Чайлд-Пью): - Хроническая сердечная недостаточность (III-IV функционального класса по классификации NYHA - Нью-Йоркской ассоциации кардиологов). С осторожностью: Подагра: гиперурикемия, т.к. АСК в низких дозах снижает экскрецию мочевой кислоты, может спровоцировать развитие подагры у предрасположенных пациентов (имеющих пониженную экскрецию мочевой кислоты): язвенная болезнь желудка и двенадцатиперстной кишки или желудочно-кишечные кровотечения в анамнезе: нарушение функции печени (ниже класса В по шкале Чайлд-Пью): нарушение функции почек (КК более 30 мл/мин): бронхиальная астма, хронические заболевания органов дыхания, сенная лихорадка, полипоз носа, лекарственная аллергия, в том числе группы НПВП: II триместр беременности: при предполагаемом хирургическом вмешательстве (включая незначительные), т.к. АСК может вызывать склонность к развитию кровотечений в течение нескольких дней после приема препарата: одновременный прием следующих препаратов: метотрексат в дозе менее 15 мг в неделю: антикоагулянты, тромболитические или антитромбоцитарные препараты: НПВП и производные салициловой кислоты в больших дозах: дигоксин: гипогликемические препараты для приема внутрь (производные сульфонилмочевины) и инсулин: вальпроевая кислота: алкоголь: селективные ингибиторы обратного захвата серотонина: ибупрофен. Беременность Применение АСК в первом триместре беременности в дозе более 300 мг в сутки может повлечь развитие дефектов у плода (пороки сердца, расщепление верхнего неба). Применение АСК в первом триместре противопоказано. Во втором триместре АСК применяют только с учетом строгой оценки риска и пользы для матери и плода, в дозах не более 150 мг в сутки и непродолжительно Применение АСК в третьем триместре беременности в дозе более 300 мг в сутки могут вызвать ослабление родовой деятельности, преждевременное закрытие артериального протока у плода, повышенную кровоточивость у матери и плода, а применение перед родами может вызвать внутричерепные кровоизлияния у новорожденного. Применение АСК в третьем триместре противопоказано. Однократный или случайный прием салицилатов в период грудного вскармливания не сопровождается развитием побочных реакций у плода и не требует прекращения грудного вскармливания. Однако при длительном применении препарата или назначении его в высоких дозах кормление грудью следует немедленно прекратить. Применение и дозы Таблетки КардиАСК® принимают 1 раз в сутки внутрь, перед едой, запивая достаточным количеством жидкости. Препарат предназначен для длительного применения. Длительность терапии определяется врачом. - При первичной профилактике острого инфаркта миокарда при наличии факторов риска: 100 мг в день или 300 мг через день: - При профилактике повторного инфаркта миокарда: 100-300 мг в день: - При нестабильной стенокардии: 100-300 мг в день: - При нестабильной стенокардии при подозрении на развитие острого инфаркта миокарда: начальная доза 100-300 мг (первую таблетку необходимо разжевать для более быстрого всасывания) должна быть принята пациентом как можно скорее после того, как возникло подозрение на развитие острого инфаркта миокарда. В последующие 30 дней после развития инфаркта миокарда должна поддерживаться доза 200-300 мг в день. Через 30 дней следует применять соответствующую терапию для профилактики повторного инфаркта миокарда. - Стабильная стенокардия: 100-300 мг в день: - Профилактика инсульта (в том числе у пациентов с преходящим нарушением мозгового кровообращения): 100-300 мг в день: - Профилактика преходящего нарушения мозгового кровообращения: 100-300 мг в день: - Профилактика тромбоэмболии после операций и инвазивных вмешательств на сосудах: 100-300 мг в день: - Профилактика тромбоза глубоких вен и тромбоэмболии легочной артерии и ее ветвей (в том числе, при длительной иммобилизации в результате обширного хирургического вмешательства): 100 - 200 мг в день или 300 мг через день. При необходимости применения АСК в дозе 100 - 200 мг возможен прием препарата КардиАСК® таблетки, покрытые пленочной кишечнорастворимой оболочкой 50 мг и 100 мг. Побочные эффекты и передозировка Побочные эффекты: Со стороны пищеварительной системы Тошнота, изжога, рвота, боли в животе, язвенные поражения слизистой оболочки желудка и двенадцатиперстной кишки, перфоративные язвы слизистой оболочки желудка и двенадцатиперстной кишки, желудочно-кишечные кровотечения, преходящие нарушения функции печени с повышением активности "печеночных" трансаминаз. Со стороны системы кроветворения Применение АСК сопровождается повышенным риском кровотечений вследствие ингибирующего действия АСК на агрегацию тромбоцитов. Зарегистрировано повышение частоты периоперационных (интра- и постоперационных) кровотечений, гематом, носовых кровотечений, кровоточивости десен, кровотечений из мочеполовых путей. Имеются сообщения о серьезных случаях кровотечений, к которым относятся желудочно-кишечные кровотечения и кровоизлияния в мозг (особенно у пациентов с артериальной гипертензией, не достигших целевых цифр артериального давления (АД) и/или получающих сопутствующую терапию антикоагулянтными препаратами), которые в отдельных случаях могут носить угрожающий жизни характер (см. раздел "Особые указания"). Кровотечения могут приводить к развитию острой или хронической постгеморрагической/железодефицитной анемии (например, вследствие скрытого кровотечения) с соответствующими клинико-лабораторными признаками и симптомами (астения, бледность, гипоперфузия). Есть сообщения о случаях гемолиза и гемолитической анемии у пациентов с тяжелыми формами дефицита глюкозо-6-фосфатдегидрогеназы. Аллергические реакции Реакции повышенной чувствительности с соответствующими клиническими и лабораторными проявлениями, такими как астматический синдром (бронхоспазм), реакции легкой и средней степени тяжести со стороны кожных покровов, дыхательных путей, желудочно-кишечного тракта и сердечно-сосудистой системы, включая такие симптомы как кожная сыпь, кожный зуд, крапивница, отек Квинке, ринит, отек слизистой оболочки носа, ринит, кардио-респираторный дистресс-синдром, тяжелые реакции, включая анафилактический шок. Со стороны центральной нервной системы Головокружение, снижение слуха, головная боль, шум в ушах, что может быть признаком передозировки препарата (см. раздел "Передозировка"). Со стороны мочевыделительной системы Есть сообщения о случаях развития нарушения функции почек и острой почечной недостаточности. Передозировка: Салицилатная интоксикация (развивается при приеме АСК в дозе более 100 мг/кг/сутки на протяжении более чем 2 суток) может явиться результатом длительного применения токсических доз препарата (хроническая интоксикация) или однократного приема токсической дозы препарата (острая интоксикация). Лечение интоксикации зависит от тяжести интоксикации и должно быть направлено на ускорение элиминации препарата и восстановления водно-электролитного баланса и кислотно-основного состояния. Симптомы передозировки от легкой до средней степени тяжести: Головокружение, шум в ушах, ухудшение слуха, повышенное потоотделение, тошнота, рвота, головная боль, спутанность сознания, тахипноэ, гипервентиляция, респираторный алкалоз. Лечение: промывание желудка, многократный прием активированного угля, форсированный щелочной диурез, восстановление водно-электролитного баланса и кислотно-основного состояния. Симптомы передозировки от средней до тяжелой степени: - респираторный алкалоз с компенсаторным метаболическим ацидозом: - гиперпирексия (крайне высокая температура тела): - нарушения дыхания: гипервентиляция, некардиогенный отек легких, угнетение дыхания, асфиксия: - нарушение сердечного ритма, артериальная гипотензия, угнетение сердечной деятельности: - нарушения водно-электролитного баланса: дегидратация, нарушение функции почек от олигурии вплоть до развития почечной недостаточности, характеризующееся гипокалиемией, гипернатриемией, гипонатриемией: - нарушение метаболизма глюкозы: гипергликемия, гипогликемия (особенно у детей), кетоацидоз: - шум в ушах, глухота: - желудочно-кишечные кровотечения: - гематологические нарушения: от ингибирования агрегации тромбоцитов до коагулопатии, удлинение протромбинового времени, гипопротромбинемия: - неврологические нарушения: токсическая энцефалопатия, угнетение функции центральной нервной системы (сонливость, спутанность сознания, кома, судороги). Лечение: немедленная госпитализация в специализированные отделения для проведения экстренной терапии - промывание желудка, многократный прием активированного угля, форсированный щелочной диурез, гемодиализ, восстановление водно-электролитного баланса и кислотно-основного состояния, симптоматическая терапия. Взаимодействие с другими ЛС: КардиАСК® при одновременном применении усиливает действие следующих препаратов: - метотрексата, за счет снижения почечного клиренса, и вытеснения его из связи с белками плазмы: комбинированное применение повышает частоту развития побочных эффектов со стороны органов кроветворения: применение препарата с метотрексатом противопоказано, если доза последнего превышает 15 мг в неделю: и возможно с осторожностью при дозе метотрексата менее 15 мг в неделю: - гепарина, непрямых антикоагулянтов, за счет нарушения функции тромбоцитов и вытеснения непрямых антикоагулянтов из связи с белками плазмы: - при одновременном применении с антикоагулянтами, тромболитическими и антиагрегантными средствами увеличивается риск кровотечения: кроме того, усиливается повреждающее действие на слизистую оболочку желудочно-кишечного тракта: - селективных ингибиторов обратного захвата серотонина, что может привести к повышению риска кровотечения из ЖКТ: - дигоксина вследствие снижения его почечной экскреции, что может привести к его передозировке: - гипогликемических препаратов для приема внутрь и инсулина за счет вытеснения производных сульфонилмочевины и связи с белками плазмы крови: - при одновременном применении с вальпроевой кислотой увеличивается ее токсичность за счет вытеснения из связи с белками плазмы крови: - НПВП и производных салициловой кислоты в высоких дозах повышается риск ульцерогенного эффекта и кровотечения из ЖКТ: - этанола (алкогольных напитков), повышается риск повреждения слизистой оболочки ЖКТ и удлинения времени кровотечения в результате синергизма действия. При необходимости одновременного применения АСК с перечисленными препаратами следует рассмотреть вопрос о необходимости уменьшения дозы указанных препаратов. АСК снижает эффект следующих препаратов: - любые диуретики (снижается скорость клубочковой фильтрации): - ингибиторы ангиотензинпревращающего фермента (АПФ) (отмечается дозозависимое снижение скорости клубочковой фильтрации, вследствие этого, ослабление гипотензивного эффекта), клинически значимое снижение скорости клубочковой фильтрации отмечается при суточной дозе АСК более 160 мг: кроме того, снижается положительное кардиопротективное действие ингибиторов АПФ при лечении хронической сердечной недостаточности. - препараты с урикозурическим действием (бензбромарон, сульфинпиразон, пробенецид). При необходимости одновременного применения АСК с этими препаратами необходима коррекция их дозы. При одновременном применении с ибупрофеном отмечается антагонизм в отношении необратимого угнетения тромбоцитов, обусловленного действием АСК, что приводит к снижению кардиопротективных эффектов АСК. Не рекомендуется сочетание АСК с ибупрофеном у пациентов с повышенным риском сердечно-сосудистых заболеваний. При одновременном применении с системными глюкокортикостероидами (ГКС), за исключением ГКС, применяемых для заместительной терапии болезни Аддисона, отмечается усиление элиминации салицилатов и соответственно, ослабление их действия. Фармакологическое действие и фармакокинетика В основе механизма антиагрегантного действия ацетилсалициловой кислоты (АСК) лежит необратимое ингибирование циклооксигеназы (ЦОГ-1), в результате чего блокируется синтез тромбоксана А2 и подавляется агрегация тромбоцитов. Антиагрегантный эффект наиболее выражен в тромбоцитах, так как они не способны повторно синтезировать циклооксигеназу. Антиагрегантный эффект сохраняется в течение 7 суток после однократного приема (больше выражен у мужчин, чем у женщин). Повышает фибринолитическую активность плазмы крови и снижает концентрацию витамина К-зависимых факторов свертывания (II, VII, IX, X). АСК оказывает также противовоспалительное, анальгезирующее и жаропонижающее действие. Фармакокинетика: После приема внутрь АСК быстро и полностью всасывается из желудочно-кишечного тракта (ЖКТ). АСК частично метаболизируется во время абсорбции. Во время и после всасывания АСК превращается в главный метаболит - салициловую кислоту, которая метаболизируется в печени под влиянием ферментов с образованием таких метаболитов, как фенилсалицилат, глюкуронида салицилат и салицилуровая кислота, обнаруживаемых во многих тканях и в моче. У женщин процесс метаболизма проходит медленнее (меньшая активность ферментов в сыворотке крови). Максимальная концентрация АСК в плазме крови достигается через 10-20 минут после приема внутрь, салициловой кислоты - через 0,3-2 часа. Вследствие того, что таблетки покрыты кислотоустойчивой оболочкой, АСК высвобождается не в желудке (оболочка эффективно блокирует растворение препарата в желудке), а в щелочной среде двенадцатиперстной кишки. Таким образом, абсорбция АСК в форме таблеток, покрытых кишечнорастворимой оболочкой, замедлена на 3-6 часов по сравнению с обычными (без оболочки) таблетками. АСК и салициловая кислота сильно связываются с белками плазмы крови (от 66 % до 98 % в зависимости от дозы) и быстро распределяются в организме. Салициловая кислота проникает через плаценту и выделяется в грудное молоко. Выведение салициловой кислоты является дозозависимым, поскольку ее метаболизм ограничен возможностями ферментативной системы. Период полувыведения (Т1/2) составляет от 2-3 часов при применении АСК в низких дозах и до 15 часов при применении препарата в высоких дозах (обычные дозы АСК в качестве анальгезирующего средства), В отличие от других салицилатов, при многократном приеме препарата негидролизированная АСК не накапливается в сыворотке крови. Салициловая кислота и ее метаболиты выводятся почками. У пациентов с нормальной функцией почек 80-100 % разовой дозы препарата выводится почками в течение 24-72 часов. Особые указания Препарат применяют по назначению врача. АСК может спровоцировать бронхоспазм, а также вызвать приступы бронхиальной астмы и другие реакции повышенной чувствительности (см. раздел "Побочное действие"). Ингибирующее действие АСК на агрегацию тромбоцитов сохраняется в течение нескольких дней после приема, в связи с чем, возможно повышение риска кровотечения в ходе оперативных вмешательств или в послеоперационном периоде. Необходимо по возможности полностью отказаться от применения АСК в предоперационном периоде. Превышение дозы АСК повышает риск желудочно-кишечного кровотечения. Передозировка особенно опасна у пациентов пожилого возраста. Влияние на способность управлять транспортными средствами: Прием препарата не влияет на способность управлять транспортными средствами и выполнять работы, требующие высокой скорости психомоторных реакций. Условия хранения и отпуска из аптек Условия хранения:В сухом, защищенном от света месте при температуре не выше 25 °С. Хранить в недоступном для детей месте. Отпуск из аптек: Без рецепта Регистрационные данные Торговое название КардиАСК® Международное непатентованное название:Ацетилсалициловая кислота. Форма выпуска:таблетки, покрытые кишечнорастворимой оболочкой. Состав:1 таблетка, покрытая кишечнорастворимой оболочкой, содержит: активное вещество: ацетилсалициловая кислота 300,0 мг: вспомогательные вещества: крахмал кукурузный 3 мг: лактоза (сахар молочный) 80 мг: целлюлоза микрокристаллическая 54 мг: Повидон (пласдон К-90) 10 мг: кальция стеарат 2 мг, полисорбат (твин 80) 1 мг: вспомогательные вещества для получения кишечнорастворимой оболочки: колликут МАЕ 100 Р 27,4 мг: коповидон (пласдон Эс-630) 3,3 мг: тальк 2,8 мг: пропиленгликоль 8,6 мг: масло касторовое 0,9 мг: титана диоксид 2 мг. АТХ: Регистрация: Лекарственное средство ЛС-002676 Фармгруппа: Нестероидный противовоспалительный препарат (НПВП)Дата регистрации: 06.03.2012. Окончание регстрации: . Описание:Таблетки, покрытые кишечнорастворимой оболочкой белого цвета, круглые, двояковыпуклой формы. Допускается легкая шероховатость и слабый запах уксусной кислоты. Упаковка:Таблетки, покрытые кишечнорастворимой оболочкой, 300 мг. По 10 или 15 таблеток в контурную ячейковую упаковку из пленки поливинилхлоридной и фольги алюминиевой печатной лакированной. По 1, 3, 10 контурных ячейковых упаковок по 10 таблеток или 2 контурные ячейковые упаковки по 15 таблеток вместе с инструкцией по применению помещают в пачку из картона. Срок годности:2 года. Не применять по истечении срока годности. Владелец рег.удостоверения:КАНОНФАРМА ПРОДАКШН, ЗАО Производитель:КАНОНФАРМА ПРОДАКШН, ЗАО. Представительство
Модель:
RUR 753
Показания Артериальная гипертензия (пациентам, которым показана комбинированная терапия амлодипином и рамиприлом в дозах, как в комбинации). Противопоказания Противопоказания Амлодипин Повышенная чувствительность к амлодипину и другим производным дигидропиридина: Тяжелая артериальная гипотензия (САД менее 90 мм рт. ст.), шок (включая кардиогенный): Обструктивный процесс, затрудняющий выброс крови из левого желудочка (например, клинически значимый стеноз аорты) Гемодинамически нестабильная сердечная недостаточность после инфаркта миокарда: Беременность: Период грудного вскармливания: Возраст до 18 лет (безопасность и эффективность не определены). Рамиприл Повышенная чувствительность к рамиприлу, другим ингибиторам ангиотензинпревращающего фермента (АПФ): Ангионевротический отек в анамнезе (наследственный или идиопатический, а также связанный с предшествующей терапией ингибиторами АПФ): Гемодинамически значимый стеноз почечных артерий (двусторонний или односторонний, в случае единственной почки): Артериальная гипотензия (систолическое артериальное давление (САД) <:90 мм.рт.ст.) или состояния с нестабильными показателями гемодинамики: Гемодинамически значимый стеноз аортального или митрального клапана, или гипертрофическая обструктивная кардиомиопатия: Первичный гиперальдостеронизм: Тяжёлая почечная недостаточность (КК<:20 мл/мин/1.73 м 2 площади поверхности тела) Гемодиализ (опыт клинического применения недостаточен): Беременность: Период грудного вскармливания: Нефропатия, лечение которой проводится глюкокортикостероидами (ГКС), нестероидными противовоспалительными препаратами (НПВП), иммуномодуляторами и/или другими цитотоксическими средствами (опыт клинического применения недостаточен): Декомпенсированная хроническая сердечная недостаточность (опыт клинического применения недостаточен): Возраст до 18 лет (опыт клинического применения недостаточен): Гемодиализ или гемофильтрация с применением некоторых мембран с отрицательно заряженной поверхностью, таких как высокопроточные мембраны из полиакрилнитрила (опасность развития реакций повышенной чувствительности): Апоферез липопротеинов низкой плотности (ЛПНП) с применением декстрана сульфата (опасность развития реакций повышенной чувствительности): Десенсибилизирующая терапия при реакциях повышенной чувствительности к ядам насекомых - пчел, ос: Острая стадия инфаркта миокарда у пациентов с такими заболеваниями как: - тяжелая сердечная недостаточность (IV функциональный класс по NYHA): - опасные для жизни желудочковые нарушения ритма сердца: - "легочное" сердце. Одновременное применение препаратов, содержащих алискирен, у пациентов с нарушением функции почек (КК менее 60 мл/мин) и пациентов с сахарным диабетом. Амлодипин+рамиприл Повышенная чувствительность к вспомогательным веществам, входящим в состав препарата: Беременность: Период грудного вскармливания: Почечная недостаточность: КК<:20 мл/мин на 1,73 м площади поверхности тела: Возраст до 18 лет (опыт клинического применения недостаточен). С осторожностью: С осторожностью применять комбинацию амлодипин+рамиприл при следующих заболеваниях и состояниях: - атеросклеротические поражения коронарных и церебральных артерий (опасность чрезмерного снижения АД): - повышение активности ренин-ангиотензин-альдостероновой системы (РААС), при котором при ингибировании АПФ имеется риск резкого снижения АД с ухудшением функции почек: - выраженная, особенно злокачественная АГ, - ХСН, особенно тяжелая или по поводу которой принимаются другие лекарственные средства (ЛС) с антигипертензивным действием, - гемодинамически значимый односторонний стеноз почечной артерии (при наличии обеих почек), - предшествующий прием диуретиков, - нарушения водно-электролитного баланса, снижение объема циркулирующей крови (ОЦК) (в том числе на фоне приема диуретиков, бессолевой диеты, диареи, рвоты, обильного потоотделения): - одновременное применение с препаратами, содержащими алискирен (при двойной блокаде РААС повышается риск резкого снижения АД, гиперкалиемии и ухудшения функции почек): - нарушения функции печени - недостаточность опыта применения: возможно как усиление, так и ослабление эффектов рамиприла: при наличии у пациентов цирроза печени с асцитом и отеками возможна значительная активация РААС: - нарушение функции почек (КК более 20 мл/мин.): - состояние после трансплантации почек: - системные заболевания соединительной ткани, в том числе системная красная волчанка, склеродермия, сопутствующая терапия препаратами, способными вызвать изменения в картине периферической крови (в том числе аллопуринолом, прокаинамидом) - возможно угнетение костномозгового кроветворения, развитие нейтропении или агранулоцитоза: - сахарный диабет - риск развития гиперкалиемии: - пожилой возраст - риск усиления антигипертензивного действия: - гиперкалиемия: - гипонатриемия: - ХСН неишемической этиологии III-IV функционального класса по классификации NYHA: - аортальный стеноз: - синдром слабости синусового узла: - митральный стеноз: - артериальная гипотензия: - единственная функционирующая почка: - реноваскулярная гипертензия: - одновременное применение дантролена, эстрамустина, калийсберегающих диуретиков и препаратов калия, калийсодержащих заменителей пищевой соли, препаратов лития: - хирургическое вмешательство/общая анестезия: - проведение гемодиализа с применением высокопроточных мембран (например, AN69®). Беременность Беременность Препарат противопоказан для применения, так как рамиприл может оказать неблагоприятное воздействие на плод: нарушение развития почек плода, снижение АД плода и новорожденных, нарушение функции почек, гиперкалиемия, гипоплазия костей черепа, олигогидрамнион, контрактура конечностей, деформация костей черепа, гипоплазия легких. Перед началом приема препарата у женщин детородного возраста следует исключить беременность. Если женщина планирует беременность, то лечение препаратом должно быть прекращено. В случае наступления беременности во время лечения препаратом следует как можно скорее прекратить его прием и перевести пациентку на прием других препаратов, при применении которых риск для ребенка будет наименьшим. Период грудного вскармливания Если лечение препаратом необходимо в период грудного вскармливания, оно должно быть прекращено (данные по выведению амлодипина и рамиприла с грудным молоком женщин отсутствуют). Фертильность Амлодипин У некоторых пациентов, получавших блокаторы кальциевых каналов, наблюдались обратимые биохимические изменения в головках сперматозоидов. Клинические данные недостаточны для оценки потенциального эффекта амлодипина на фертильность. Применение и дозы Применять Эгипрес внутрь, по 1 капсуле 1 раз в сутки, в одно и то же время, вне зависимости от приёма пищи. Доза препарата Эгипрес подбирается после ранее проведенного титрования доз отдельных компонентов препарата: рамиприла и амлодипина у пациентов с АЕ. Препарат Эгипрес с фиксированными дозами активных компонентов не может применяться для начальной терапии. Если больным необходима коррекция доз, то её следует проводить только с помощью титрации доз активных компонентов в монотерапии. Только после этого возможно применение препарата Эгипрес с фиксированными дозами активных компонентов в нижеприведенных комбинациях. При терапевтической необходимости доза препарата Эгипрес может быть изменена на основании индивидуального титрования доз отдельных компонентов: 2,5 мг амлодипина + 2,5 мг рамиприла или 5 мг амлодипина + 5 мг рамиприла или 5 мг амлодипина + 10 мг рамиприла или 10 мг амлодипина + 5 мг рамиприла или 10 мг амлодипина + 10 мг рамиприла. Эгипрес в дозе 10 мг амлодипина + 10 мг рамиприла является максимальной суточной дозой препарата, которую не рекомендуется превышать. Дозировки 10 мг амлодипина + 5 мг рамиприла (по амлодипину) и 5 мг амлодипина + 10 мг рамиприла (по рамиприлу) являются максимальными суточными дозами. Взрослые У пациентов, принимающих диуретики, препарат следует назначать с осторожностью, вследствие риска нарушения водно-электролитного баланса. У этих пациентов следует контролировать функцию почек и содержание калия в крови. Пациенты пожилого возраста и пациенты с почечной недостаточностью Выведение амлодипина и рамиприла и его метаболитов у пациентов пожилого возраста и пациентов с почечной недостаточностью замедлено. Поэтому у таких пациентов необходимо регулярно контролировать содержание креатинина и калия в плазме крови. Эгипрес может назначаться пациентам с КК равным или превышающем 60 мл/мин. При КК<:60 мл/мин, а также у пациентов с АГ, находящихся на гемодиализе, Эгипрес рекомендуется только пациентам, получавшим 2.5 мг или 5 мг рамиприла как оптимальную поддерживающую дозу по ходу титрования индивидуальной дозы. Нет необходимости титрования индивидуальной дозы амлодипина у пациентов с нарушением функции почек. Эгипрес противопоказан пациентам с КК<:20 мл/мин/1.73 м площади поверхности тела. Изменение концентрации амлодипина в плазме крови не коррелирует со степенью выраженности почечной недостаточности. Пациенты с печеночной недостаточностью Следует соблюдать осторожность при назначении препарата Эгипрес пациентам с печеночной недостаточностью из-за отсутствия рекомендаций по дозированию препарата у таких пациентов. Эгипрес рекомендуется только пациентам, получавшим 2.5 мг рамиприла как оптимальную поддерживающую дозу по ходу титрования индивидуальной дозы. Дети и подростки Эгипрес не следует назначать детям и подросткам до 18 лет из-за отсутствия данных об эффективности и безопасности применения рамиприла и амлодипина у данных групп пациентов как в виде монотерапии, так и в виде комбинированной терапии. Побочные эффекты и передозировка Побочные эффекты: Указанные ниже нежелательные эффекты даются в соответствии со следующими градациями частоты их возникновения по классификации ВОЗ: очень частые: более 1/10 (более 10%): частые: более 1/100 но менее 1/10 (более 1%, но менее 10%): нечастые: более 1/1000 но менее 1/100 (более 0,1%, но менее 1%): редкие: более 1/10000 но менее 1/1000 (более 0,01%, но менее 0,1%): очень редкие: менее 1/10000 (менее 0,01%). Амлодипин Со стороны ССС: часто - периферические отеки (лодыжек и стоп), ощущение сердцебиения: нечасто - чрезмерное снижение АД, ортостатическая гипотензия, васкулит: редко - развитие или усугубление СН: очень редко - нарушения ритма сердца (включая брадикардию, желудочковую тахикардию и мерцание предсердий), ИМ, боли в грудной клетке, мигрень. Со стороны опорно-двигательного аппарата и соединительной ткани: нечасто - артралгия, судороги мышц, миалгия, боль в спине, артроз: редко - миастения. Со стороны ЦНС и периферической нервной системы: часто - ощущение жара и приливов крови к коже лица, повышенная утомляемость, головокружение, головная боль, сонливость: нечасто - недомогание, обморок, повышенное потоотделение, астения, гипестезии, парестезии, периферическая нейропатия, тремор, бессонница, лабильность настроения, необычные сновидения, нервозность, депрессия, тревога: редко - судороги, апатия: очень редко - атаксия, амнезия, зарегистрированы отдельные случаи экстрапирамидного синдрома. Со стороны пищеварительной системы: часто - боль в брюшной полости, тошнота: нечасто - рвота, изменения режима дефекации (включая запор, метеоризм), диспепсия, диарея, анорексия, сухость слизистой оболочки полости рта, жажда: редко - гиперплазия десен, повышение аппетита: очень редко - гастрит, панкреатит, гипербилирубинемия, желтуха (обычно холестатическая), повышение активности "печеночных" трансаминаз, гепатит. Со стороны крови: очень редко - тромбоцитопеническая пурпура, тромбоцитопения, лейкопения. Метаболические нарушения: очень редко - гипергликемия. Со стороны дыхательной системы: нечасто - одышка, ринит: очень редко - кашель. Со стороны почек и мочевыводящих путей: нечасто - учащенное мочеиспускание, болезненное мочеиспускание, никтурия, импотенция: очень редко - дизурия, полиурия. Аллергические реакции: нечасто - кожный зуд, сыпь: очень редко - ангионевротический отек, мультиформная эритема, крапивница. Прочие: нечасто - алопеция, "звон" в ушах, гинекомастия, увеличение/снижение массы тела, нарушение зрения, диплопия, нарушение аккомодации, ксерофтальмия, конъюнктивит, боль в глазах, извращение вкуса, озноб, носовое кровотечение: редко - дерматит: очень редко - паросмия, ксеродермия, "холодный" пот, нарушение пигментации кожи. Рамиприл Со стороны сердца: нечасто - ишемия миокарда, включая развитие приступа стенокардии или ИМ, тахикардия, аритмии (появление или усиление), ощущение сердцебиения, периферические отеки. Со стороны сосудов: часто - чрезмерное снижение АД, нарушение ортостатической регуляции сосудистого тонуса (ортостатическая гипотензия), синкопальные состояния: нечасто - "приливы" крови к коже лица: редко - возникновение или усиление нарушений кровообращения на фоне стенозирующих сосудистых поражений, васкулит: частота неизвестна - синдром Рейно. Со стороны центральной нервной системы (ЦНС): часто - головная боль, ощущение "легкости" в голове: нечасто - головокружение, агевзия (утрата вкусовой чувствительности), дисгевзия (нарушение вкусовой чувствительности), парестезии (ощущение жжения): редко - тремор, нарушение равновесия: частота неизвестна - ишемия головного мозга, включая ишемический инсульт и преходящее нарушение мозгового кровообращения, нарушение психомоторных реакций, паросмия (нарушение восприятия запахов). Со стороны органа зрения: нечасто - нарушения зрения, включая нечеткость зрительного восприятия: редко - конъюнктивит. Нарушения со стороны органа слуха: редко - нарушения слуха, звон в ушах. Со стороны психики: нечасто - подавленное настроение, тревога, нервозность, двигательное беспокойство, нарушения сна, включая сонливость: редко - спутанность сознания: частота неизвестна - нарушение концентрации внимания. Со стороны дыхательной системы: часто - "сухой" кашель (усиливающийся по ночам и в положении лежа), бронхит, синусит, одышка: нечасто - бронхоспазм, включая утяжеление течения бронхиальной астмы, заложенность носа. Со стороны пищеварительной системы: часто - воспалительные реакции в желудке и кишечнике, расстройства пищеварения, ощущение дискомфорта в области живота, диспепсия, диарея, тошнота, рвота: нечасто - панкреатит, в т.ч. и с летальным исходом (случаи панкреатита с летальным исходом при приеме ингибиторов АПФ наблюдались крайне редко), повышение активности ферментов поджелудочной железы в плазме крови, интестинальный ангионевротический отек, боли в животе, гастрит, запор, сухость слизистой оболочки полости рта: редко - глоссит: частота неизвестна - афтозный стоматит (воспалительная реакция слизистой оболочки полости рта). Со стороны гепатобилиарной системы: нечасто - повышение активности "печеночных" ферментов и содержания конъюгированного билирубина в плазме крови: редко - холестатическая желтуха, гепатоцеллюлярные поражения: частота неизвестна - острая печеночная недостаточность, холестатический или цитолитический гепатит (летальный исход наблюдался крайне редко). Со стороны почек и мочевыводящих путей: нечасто - нарушение функции почек, включая развитие острой почечной недостаточности, увеличение выделения количества мочи, усиление ранее существовавшей протеинурии, повышение концентрации мочевины и креатинина в крови. Со стороны репродуктивной системы и молочных желез: нечасто - преходящая импотенция за счет эректильной дисфункции, снижение либидо: частота неизвестна - гинекомастия. Со стороны крови и лимфатической системы: нечасто - эозинофилия: редко - лейкопения, включая нейтропению и агранулоцитоз, уменьшение количества эритроцитов в периферической крови, снижение гемоглобина, тромбоцитопения: частота неизвестна - угнетение костно-мозгового кроветворения, панцитопения, гемолитическая анемия. Со стороны кожных покровов и слизистых оболочек: часто - кожная сыпь, в частности, макулопапулезная: нечасто - ангионевротический отек, в т.ч. и с летальным исходом (отек гортани может вызвать обструкцию дыхательных путей, приводящую к летальному исходу), кожный зуд, гипергидроз (повышенное потоотделение): редко - эксфолиативный дерматит, крапивница, онихолизис: очень редко - реакции фотосенсибилизации: частота неизвестна - токсический эпидермальный некролиз, синдром Стивенса-Джонсона, мультиформная эритема, пемфигус, утяжеление течения псориаза, псориазоподобный дерматит, пемфигоидная или лихеноидная (лишаевидная) экзантема или энантема, алопеция. Со стороны опорно-двигательного аппарата и соединительной ткани: часто - мышечные судороги, миалгия: нечасто - артралгия. Со стороны обмена веществ, питания и лабораторных показателей: часто - повышение содержания калия в крови: нечасто - анорексия, снижение аппетита: частота неизвестна - снижение концентрации натрия в крови, синдром неадекватной секреции анти- диуретического гормона. Со стороны иммунной системы, частота неизвестна - анафилактические или анафилактоидные реакции (при ингибировании АПФ увеличивается количество анафилактических или анафилактоидных реакций на яды насекомых), повышение титра антинуклеарных антител. Общие нарушения: часто - боли в груди, чувство усталости: нечасто - повышение температуры тела: редко - астения (слабость). Передозировка: Информация о передозировке препарата Эгипрес отсутствует. Амлодипин Симптомы: выраженное снижение АД с возможным развитием рефлекторной тахикардии и чрезмерной периферической вазодилатации (существует вероятность появления выраженной и стойкой артериальной гипотензии, в том числе с развитием шока и летального исхода). Лечение: Назначение активированного угля (особенно в первые 2 часа после передозировки), промывание желудка, придание возвышенного положения конечностям, активное поддержание функций ССС, мониторинг показателей работы сердца и легких, контроль за ОЦК и диурезом. Для восстановления тонуса сосудов и АД, если нет противопоказаний, может оказаться полезным применение сосудосуживающих препаратов. Используют внутривенное введение глюконата кальция. Амлодипин в значительной степени связывается с белками сыворотки крови, поэтому гемодиализ малоэффективен. Рамиприл Симптомы: чрезмерная периферическая вазодилатация с развитием выраженного снижения АД, шока: брадикардия или рефлекторная тахикардия, водно-электролитные нарушения, острая почечная недостаточность, ступор. Лечение: промывание желудка, назначение адсорбентов, натрия сульфата (по возможности в течение первых 30 мин). В случае выраженного снижения АД пациента следует уложить, ноги приподнять, активно поддерживать функции ССС: к терапии по восполнению ОЦК и восстановлению электролитного баланса дополнительно может быть добавлено введение альфа 1-адренергических агонистов (норэпинефрин, допамин) и ангиотензинамида. В случае рефрактерной к медикаментозному лечению брадикардии может потребоваться установка временного искусственного водителя ритма. При передозировке необходимо мониторировать содержание креатинина и электролитов в сыворотке крови. Рамиприлат плохо выводится из крови с помощью гемодиализа. Взаимодействие с другими ЛС: Амлодипин Можно ожидать, что ингибиторы ферментов микросомального окисления печени (эритромицин у молодых, дилтиазем у пожилых, кетоконазол, итраконазол, ритонавир) будут повышать концентрацию амлодипина в плазме крови, усиливая риск побочных эффектов, а индукторы ферментов микросомального окисления печени - уменьшать. При одновременном применении амлодипина с циметидином фармакокинетика амлодипина не меняется. Одновременный однократный прием 240 мл грейпфрутового сока и 10 мг амлодипина внутрь не сопровождается существенным изменением фармакокинетики амлодипина. В отличие от других блокаторов "медленных" кальциевых каналов (БМКК), не было обнаружено клинически значимого взаимодействия амлодипина (III поколение БМКК) при совместном применении с НПВП, особенно индометацином. Возможно усиление антиангинального и антигипертензивного действия БМКК при совместном применении с тиазидными и "петлевыми" диуретиками, верапамилом, ингибиторами АПФ, бета-адреноблокаторами и нитратами, а также повышение их антигипертензивного действия при совместном применении с альфа 1-адреноблокаторами, нейролептиками. Хотя при изучении амлодипина отрицательного инотропного эффекта обычно не наблюдали, тем не менее, некоторые БМКК могут усиливать выраженность отрицательного инотропного действия антиаритмических препаратов, вызывающих удлинение интервала QT (например, амиодарон и хинидин). При совместном применении БМКК с препаратами лития (для амлодипина данные отсутствуют), возможно усиление проявления их нейротоксичности (тошнота, рвота, диарея, атаксия, тремор, шум в ушах). Амлодипин не влияет in vitro на степень связывания с белками плазмы крови дигоксина, фенитоина, варфарина и индометацина. Однократный прием алюминий/магний-содержащих антацидов не оказывает существенного влияния на фармакокинетику амлодипина. Однократный прием 100 мг силденафила у больных эссенциальной гипертензией не оказывает влияния на параметры фармакокинетики амлодипина. Повторное применение амлодипина в дозе 10 мг и аторвастатина в дозе 80 мг не сопровождается значительными изменениями показателей фармакокинетики аторвастатина. При одновременном применении амлодипина с дигоксином у здоровых добровольцев содержание дигоксина в сыворотке и его почечный клиренс не изменяются. При однократном и повторном применении в дозе 10 мг амлодипин не оказывает существенного влияния на фармакокинетику этанола. Амлодипин не влияет на изменение протромбинового времени, вызванное варфарином. Амлодипин не вызывает значительных изменений фармакокинетики циклоспорина. Не рекомендуемые комбинации Одновременное применение дантролена (в/в введение), индукторов изоферментов системы цитохрома СУРЗА4 (например, рифампицин, препараты Зверобоя продырявленного) и ингибиторов изоферментов системы цитохрома СУРЗА4 (ингибиторы протеазы, противогрибковые препараты группы азолов, макролиды, например, эритромицин или кларитромицин, верапамил или дилтиазем). Рамиприл Противопоказанные комбинации Применение некоторых высокопроточных мембран с отрицательно заряженной поверхностью (например, полиакрилнитрильных мембран) при проведении гемодиализа или гемофильтрации: применение декстрана сульфата при аферезе ЛПНП - риск развития тяжелых анафилактических реакций. Нерекомендуемые комбинации С солями калия, калийсберегающими диуретиками (например, амилоридом, триамтереном, спиронолактоном) и другими препаратами (в том числе с антагонистами рецепторов ангиотензина II (АРА II), с триметопримом, такролимусом, циклоспорином) - возможно развитие гиперкалемии (при одновременном применении требуется регулярный контроль содержания калия в сыворотке крови). Комбинации, которые следует применять с осторожностью С антигипертензивными средствами (особенно диуретиками) и другими препаратами, снижающими АД (нитратами, трициклическими антидепрессантами, средствами для общей и местной анестезии, этанолом, баклофеном, алфузозином, доксазозином, празозином, тамсулозином, теразозином) - потенцирование антигипертензивного эффекта. При комбинации с диуретиками следует контролировать содержание натрия в сыворотке крови. Со снотворными, наркотическими и обезболивающими средствами - возможно более выраженное снижение АД. С вазопрессорными симпатомиметиками (эпинефрином, изопротеренолом, добутамином, допамином) - уменьшение антигипертензивного действия рамиприла, требуется регулярный контроль АД. С аллопуринолом, прокаинамидом, цитостатиками, иммунодепрессантами, системными ГКС и другими средствами, которые могут влиять на гематологические показатели - совместное применение увеличивает риск развития лейкопении. С солями лития - повышение содержания лития в сыворотке и усиление кардио- и нейротоксического действия лития. С гипогликемическими средствами для приема внутрь (производными сульфонилмочевины, бигуанидами), инсулином - в связи с уменьшением инсулинорезистентности под влиянием рамиприла возможно усиление гипогликемического эффекта этих препаратов, вплоть до развития гипогликемии. Одновременное применение препаратов, содержащих алискирен, у пациентов с сахарным диабетом и почечной недостаточностью (КК менее 60 мл/мин), а также с вилдаглиптином - в связи с увеличением частоты развития ангионевротического отека при одновременном применении с ингибиторами АПФ. Комбинации, которые следует принимать во внимание С НПВП (индометацин, ацетилсалициловая кислота) - возможно ослабление действия рамиприла, повышение риска нарушения функции почек и повышения содержания калия в сыворотке крови. С гепарином - возможно повышение содержания калия в сыворотке крови. С натрия хлоридом - ослабление антигипертензивного действия рамиприла и менее эффективное лечение симптомов ХСН. С этанолом - усиление симптомов вазодилатации. Рамиприл может усиливать неблагоприятное воздействие этанола на организм. С эстрогенами - ослабление антигипертензивного действия рамиприла (задержка жидкости). Десенсибилизирующая терапия при повышенной чувствительности к ядам насекомых - ингибиторы АПФ, включая рамиприл, увеличивают вероятность развития тяжелых анафилактических или анафилактоидных реакций на яды насекомых. Фармакологическое действие и фармакокинетика Амлодипин Амлодипин - производное дигидропиридина. Связываясь с дигидропиридиновыми рецепторами, блокирует "медленные" кальциевые каналы, ингибирует трансмембранный переход кальция внутрь клеток гладких мышц сосудов и сердца (в большей степени - в гладкомышечные клетки сосудов, чем в кардиомиоциты). Оказывает антигипертензивный и антиангинальный эффекты. Механизм антигипертензивного действия амлодипина обусловлен прямым расслабляющим влиянием на гладкие мышцы сосудов. Амлодипин уменьшает ишемию миокарда следующими двумя путями: - Расширяет периферические артериолы и, таким образом, снижает ОПСС (постнагрузку), при этом ЧСС практически не изменяется, что приводит к снижению потребления энергии и потребности миокарда в кислороде. - Расширяет коронарные и периферические артерии и артериолы как в нормальных, так и в ишемизированных зонах миокарда, что увеличивает поступление кислорода в миокард у пациентов с вазоспастической стенокардией (стенокардия Принцметала) и предотвращает развитие коронароспазма, вызванного курением. У пациентов с АГ суточная доза амлодипина обеспечивает снижение АД на протяжении 24 ч (как в положении на спине, так и стоя). Благодаря медленному началу действия, амлодипин не вызывает резкого снижения АД. У пациентов со стенокардией разовая суточная доза препарата увеличивает продолжительность выполнения физической нагрузки, задерживает развитие очередного приступа стенокардии и депрессии сегмента ST (на 1 мм) на фоне физической нагрузки, снижает частоту приступов стенокардии и потребность в нитроглицерине. Применение амлодипина у пациентов с ИБС У пациентов с заболеваниями ССС (включая коронарный атеросклероз с поражением от одного сосуда и до стеноза 3 и более артерий и атеросклероза сонных артерий), перенесших ИМ, чрезкожную транслюминальную ангиопластику коронарных артерий (ТЛП) или страдающих стенокардией) применение амлодипина предупреждает развитие утолщения интимы-медии сонных артерий, значительно снижает летальность от сердечнососудистых причин, ИМ, инсульта, ТЛП, аорто-коронарного шунтирования, приводит к снижению числа госпитализаций по поводу нестабильной стенокардии и прогрессирования ХСН, снижает частоту вмешательств, направленных на восстановление коронарного кровотока. Применение амлодипина у пациентов с СП. Амлодипин не повышает риск смерти или развития осложнений и смертельных исходов у пациентов с ХСН III-IV ФК по NYHA на фоне терапии дигоксином, диуретиками и ингибиторами АИФ. У пациентов с ХСН III-IV ФК по NYHA неишемической этиологии при применении амлодипина существует вероятность возникновения отека легких. Амлодипин не вызывает неблагоприятных метаболических эффектов, в том числе он не влияет на содержание показателей липидного профиля. Рамиприл Рамиприлат, образующийся при участии "печеночных" ферментов активный метаболит рамиприла, является длительно действующим ингибитором фермента дипептидилкарбоксипептидазы I (синонимы: ангиотензинпревращающий фермент (АИФ), кининаза II). В плазме крови и в тканях этот фермент кининаза II катализирует превращение ангиотензина I в активное сосудосуживающее вещество - ангиотензин II, а также способствует распаду брадикинина. Снижение образования ангиотензина II и ингибирование распада брадикинина приводит к расширению сосудов и снижению артериального давления (АД). Повышение активности калликреин-кининовой системы в крови и тканях обуславливает кардиопротективное и эндотелиопретективное действие рамиприла за счет активации простагландиновой системы и, соответственно, увеличения синтеза простагландинов (ПГ), стимулирующих образование оксида азота (N0) в эндотелиоцитах. Ангиотензин II стимулирует выработку альдостерона, поэтому прием рамиприла приводит к снижению секреции альдостерона и повышению содержания ионов калия в сыворотке. При снижении содержания ангиотензина II в крови устраняется его ингибирующее влияние на секрецию ренина по типу отрицательной обратной связи, что приводит к повышению активности ренина плазмы крови. Предполагается, что развитие некоторых нежелательных реакций (в частности, "сухого" кашля) связано с повышением активности брадикинина. У пациентов с артериальной гипертензией (АГ) прием рамиприла приводит к снижению АД в положении на спине и стоя, без компенсаторного увеличения частоты сердечных сокращений (ЧСС). Рамиприл значительно снижает общее периферическое сопротивление сосудов (ОПСС), практически не вызывая изменений в почечном кровотоке и скорости клубочковой фильтрации. Антигипертензивное действие начинает проявляться через 1-2 ч после приема внутрь разовой дозы препарата, достигая наибольшего значения через 3-6 ч, и сохраняется в течение 24 ч. При курсовом приеме антигипертензивный эффект может постепенно увеличиваться, стабилизируясь обычно к 3-4 неделе регулярного приема препарата и затем сохраняясь в течение длительного времени. Внезапное прекращение приема препарата не приводит к быстрому и значительному повышению АД (отсутствие синдрома "отмены"). У пациентов с АГ рамиприл замедляет развитие и прогрессирование гипертрофии миокарда и сосудистой стенки. У пациентов с хронической сердечной недостаточностью (ХСН) рамиприл снижает ОПСС (уменьшение постнагрузки на сердце), увеличивает емкость венозного русла и снижает давление наполнения левого желудочка (ЛЖ), что, соответственно, приводит к уменьшению преднагрузки на сердце. У этих пациентов при приеме рамиприла наблюдается увеличение сердечного выброса, фракции выброса и улучшение переносимости физической нагрузки. При диабетической и недиабетической нефропатии прием рамиприла замедляет скорость прогрессирования почечной недостаточности и время наступления терминальной стадии почечной недостаточности и, благодаря этому, уменьшает потребность в процедурах гемодиализа или трансплантации почки. При начальных стадиях диабетической или недиабетической нефропатии рамиприл уменьшает степень выраженности альбуминурии. У пациентов с высоким риском развития заболеваний сердечно-сосудистой системы (ССС) вследствие наличия сосудистых поражений (диагностированная ишемическая болезнь сердца (ИБС), облитерирующие заболевания периферических артерий в анамнезе, инсульт в анамнезе) или сахарного диабета с не менее чем одним дополнительным фактором риска (микроальбуминурия, АГ, увеличение содержания общего холестерина, снижение содержания холестерина липопротеинов высокой плотности (ЛПВП), курение) добавление рамиприла к стандартной терапии значительно снижает частоту развития инфаркта миокарда (ИМ), инсульта и смертности от сердечно-сосудистых причин. Кроме этого, рамиприл снижает показатели общей смертности, а также потребность в процедурах реваскуляризации, замедляет возникновение или прогрессирование ХСН. У пациентов с сердечной недостаточностью (СН), развившейся в первые дни острого инфаркта миокарда (ОИМ) (2-9 сутки), при приеме рамиприла, начиная с 3 по 10 сутки ОИМ, снижается риск показателя смертности (на 27%), риск внезапной смерти (на 30%), риск прогрессирования ХСН до тяжелой - III-IV функциональный класс (ФК) по классификации Нью-Йоркской ассоциации кардиологов (NYHA) - резистентной к терапии (на 27%), вероятность последующей госпитализации из-за развития СН (на 26%). В общей популяции пациентов, а также у пациентов с сахарным диабетом, как с АГ, так и с нормальными показателями АД, рамиприл значительно снижает риск развития нефропатии и возникновения микроальбуминурии. Фармакокинетика: Амлодипин После приема внутрь в терапевтических дозах амлодипин хорошо абсорбируется, время достижения максимальной концентрации в плазме крови (ТСmах) при пероральном приеме составляет 6-12 ч. Абсолютная биодоступность оставляет 64-80%. Vd составляет примерно 21 л/кг. Связь с белками плазмы крови составляет примерно 97,5%. Прием пищи не влияет на всасывание амлодипина. Препарат проникает через гематоэнцефалический барьер. Т1/2 из плазмы крови составляет около 35-50 ч, что соответствует назначению препарата один раз в сутки. У пациентов с печеночной недостаточностью и тяжелой ХСН Т1/2 увеличивается до 56-60 ч. Общий клиренс - 0,43 л/ч/кг. Стабильная Css (5-15 нг/мл) достигается через 7-8 дней постоянного приема амлодипина, он метаболизируется в печени с образованием неактивных метаболитов. 10% исходного препарата и 60% метаболитов выводится почками, а 20% - через кишечник. Выведение с грудным молоком неизвестно. В ходе гемодиализа амлодипин не удаляется. Применение у больных почечной недостаточностью Т1/2 из плазмы крови у больных с почечной недостаточностью увеличивается до 60 ч. Изменение концентрации амлодипина в плазме крови не коррелирует со степенью нарушения функции почек. Применение у пожилых пациентов У пожилых пациентов ТСmах и Сmах амлодипина практически не отличаются от таковых у более молодых пациентов. У пациентов пожилого возраста, страдающих ХСН, отмечена тенденция к снижению клиренса амлодипина, что приводит к увеличению AUC и Т1/2 до 65 ч. Рамиприл После приема внутрь рамиприл быстро всасывается из желудочно-кишечного тракта (ЖКТ) (50-60%). Прием пищи замедляет его абсорбцию, но не влияет на степень всасывания. Рамиприл подвергается интенсивному пресистемному метаболизму/активации (главным образом, в печени путем гидролиза), в результате которого образуется его единственный активный метаболит - рамиприлат, активность которого в отношении ингибирования АПФ примерно в 6 раз превышает активность рамиприла. Кроме этого, в результате метаболизма рамиприла образуется не обладающий фармакологической активностью дикетопиперазин, который затем подвергается конъюгации с глюкуроновой кислотой. Рамиприлат также глюкуронируется и метаболизируется до дикетопиперазиновой кислоты. Биодоступность рамиприла после приема внутрь колеблется от 15% (для дозы 2,5 мг) до 28% (для дозы 5 мг). Биодоступность рамиприлата после приема внутрь 2,5 мг и 5 мг рамиприла составляет приблизительно 45% (по сравнению с его биодоступностью после внутривенного введения в тех же дозах). После приема рамиприла внутрь максимальные концентрации в плазме крови (Стmах) рамиприла и рамиприлата достигаются через 1 и 2-4 ч, соответственно. Снижение концентрации рамиприлата в плазме крови происходит в несколько этапов: фаза распределения и выведения с периодом полувыведения (Т1/2) рамиприлата, составляющим приблизительно 3 ч, затем промежуточная фаза с Т1/2 рамиприлата, составляющим приблизительно 15 ч, и конечная фаза с очень низкой концентрацией рамиприлата в плазме крови и Т1/2 рамиприлата, составляющим приблизительно 4-5 дней. Эта конечная фаза обусловлена медленным высвобождением рамиприлата из прочной связи с рецепторами АПФ. Несмотря на продолжительную конечную фазу при однократном в течение суток приеме рамиприла внутрь в дозе 2,5 мг и более, равновесная плазменная концентрация (Css) рамиприлата достигается приблизительно через 4 дня лечения. При курсовом назначении препарата "эффективный" Т1/2 в зависимости от дозы составляет 13-17 ч. Связывание с белками плазмы крови приблизительно составляет для рамиприла 73%, а для рамиприлата - 56%. После внутривенного (в/в) введения объемы распределения (Vd) рамиприла и рамиприлата составляют приблизительно 90 и 500 л, соответственно. После приема внутрь меченного радиоактивным изотопом рамиприла (10 мг) 39% радиоактивности выводится через кишечник и около 60% - почками. После в/в введения рамиприла, 50-60% дозы обнаруживается в моче в виде рамиприла и его метаболитов. После в/в введения рамиприлата около 70% дозы обнаруживается в моче в виде рамиприлата и его метаболитов, иначе говоря, при в/в введении рамиприла и рамиприлата значительная часть дозы выводится через кишечник с желчью, минуя почки (50 и 30%, соответственно). После приема внутрь 5 мг рамиприла у пациентов с дренированием желчных протоков практически одинаковые количества рамиприла и его метаболитов выделяются почками и через кишечник в течение первых 24 ч после приема. Приблизительно 80-90% метаболитов в моче и желчи были идентифицированы как рамиприлат и метаболиты рамиприлата. Рамиприла глюкуронид и рамиприла дикетопиперазин составляют приблизительно 10-20% от общего количества, а содержание в моче неметаболизированного рамиприла составляет приблизительно 2%. При нарушениях функции почек с клиренсом креатинина (КК) менее 60 мл/мин выведение рамиприлата и его метаболитов почками замедляется. Это приводит к повышению концентрации рамиприлата в плазме крови, которая снижается медленнее, чем у пациентов с нормальной функцией почек. При приеме рамиприла в высоких дозах (10 мг) нарушение функции печени приводит к замедлению пресистемного метаболизма рамиприла до активного рамиприлата и более медленному выведению рамиприлата. У здоровых добровольцев и у пациентов с АГ после 2 недель лечения рамиприлом в суточной дозе 5 мг не наблюдается клинически значимого накопления рамиприла и рамиприлата. У пациентов с ХСН после 2 недель лечения рамиприлом в суточной дозе 5 мг отмечается 1,5-1,8-кратное увеличение концентраций рамиприлата в плазме крови и площади под фармакокинетической кривой концентрации вещества в плазме в зависимости от времени (AUC). У здоровых добровольцев пожилого возраста (65-76 лет) фармакокинетика рамиприла и рамиприлата существенно не отличается от таковой у молодых здоровых добровольцев. Особые указания Особые указания, относящиеся к рамиприлу и амлодипину, применимы к препарату Эгипрес. Особые указания, относящиеся к приему амлодипина При лечении АГ амлодипин может сочетаться с приемом тиазидных диуретиков, альфа- и бета-адреноблокаторов, ингибиторов АПФ, нитратов пролонгированного действия, сублингвальным нитроглицерином, НПВП, антибиотиками и гипогликемическими средствами для приема внутрь. При лечении стенокардии амлодипин можно назначать в комбинации с другими антиангинальными средствами, в том числе у пациентов, рефрактерных к лечению нитратами и/или бета-адреноблокаторами в адекватных дозах. Амлодипин не оказывает какого-либо неблагоприятного влияния на обмен веществ и липиды плазмы крови и может применяться при лечении пациентов с бронхиальной астмой, сахарным диабетом и подагрой. Амлодипин может быть применен и в тех случаях, когда пациент предрасположен к вазоспазму/вазоконстрикции. Пациентам с малой массой тела, невысокого роста и пациентам с выраженным нарушением функций печени может потребоваться меньшая дозировка. Во время лечения необходим контроль массы тела и наблюдение у стоматолога (для предотвращения болезненности, кровоточивости и гиперплазии десен). Особые указания, относящиеся к приему рамиприла Перед началом лечения рамиприлом необходимо устранить гипонатриемию и гиповолемию. Пациентам, ранее принимавшим диуретики, необходимо их отменить или, по крайней мере, снизить их дозу за 2-3 дня до начала приема рамиприла (в этом случае следует регулярно контролировать состояние пациентов с ХСН, в связи с возможностью развития у них декомпенсации при увеличении ОЦК). После приема первой дозы препарата, а также при увеличении его дозы и/или дозы диуретиков (особенно "петлевых"), необходимо обеспечить регулярное медицинское наблюдение за пациентом в течение не менее 8 ч для своевременного принятия соответствующих мер в случае чрезмерного снижения АД. Если рамиприл используется впервые или в высокой дозе у пациентов с повышенной активностью РААС, то у них следует регулярно контролировать АД, особенно в начале лечения, т.к. у этих пациентов имеется повышенный риск чрезмерного снижения АД. При злокачественной АГ и СН, в особенности в острой стадии ИМ, лечение с применением рамиприла следует начинать только в условиях стационара. У пациентов с ХСН прием препарата может привести к развитию выраженного снижения АД, которое в ряде случаев сопровождается олигурией или азотемией и редко - развитием острой почечной недостаточности. Следует соблюдать осторожность при лечении пожилых пациентов, т.к. они могут быть особенно чувствительны к ингибиторам АПФ: в начальной фазе лечения рекомендуется контролировать показатели функции почек. У пациентов, для которых снижение АД может представлять определенный риск (например, у пациентов с атеросклеротическим сужением коронарных или мозговых артерий), лечение должно начинаться под строгим медицинским наблюдением. Следует соблюдать осторожность при физической нагрузке и/или жаркой погоде из-за риска повышенного потоотделения и дегидратации с развитием артериальной гипотензии вследствие уменьшения ОЦК и снижения содержания натрия в крови. Во время лечения не рекомендуется употреблять алкоголь. Преходящая артериальная гипотензия не является противопоказанием для продолжения лечения после стабилизации АД. В случае повторного возникновения выраженной артериальной гипотензии следует уменьшить дозу или отменить препарат. У пациентов, получавших лечение ингибиторами АПФ, наблюдались случаи ангионевротического отека лица, конечностей, губ, языка, глотки или гортани. При возникновении отечности в области лица (губы, веки) или языка, либо нарушении глотания или дыхания, пациент должен немедленно прекратить прием препарата. Ангионевротический отек, локализующийся в области языка, глотки, или гортани (возможные симптомы: нарушение глотания или дыхания), может угрожать жизни и требует проведения неотложных мер по его купированию: подкожное введение 0,3-0,5 мг или внутривенное капельное введение 0,1 мг эпинефрина (под контролем АД, ЧСС и ЭКГ) с последующим применением ГКС (в/в, в/м, или внутрь): также рекомендуется внутривенное введение антигистаминных средств (антагонистов H1- и Н2-гистаминовых рецепторов), а в случае недостаточности инактиваторов фермента C1-эстеразы можно рассмотреть вопрос о необходимости введения в дополнение к эпинефрину ингибиторов фермента C1-эстеразы. Пациент должен быть госпитализирован, и наблюдение за ним должно проводиться до полного купирования симптомов, но не менее 24 ч. У пациентов, получавших ингибиторы АПФ, наблюдались случаи интестинального ангионевротического отека, который проявлялся болями в животе с тошнотой и рвотой или без них: в некоторых случаях одновременно наблюдался и ангионевротический отек лица. При появлении у пациента на фоне лечения ингибиторами АПФ вышеописанных симптомов следует при проведении дифференциального диагноза рассматривать и возможность развития у них интестинального ангионевротического отека. Лечение, направленное на десенсибилизацию к яду насекомых (пчелы, осы), и одновременный прием ингибиторов АПФ могут инициировать анафилактические и анафилактоидные реакции (например, снижение АД, одышку, рвоту, аллергические кожные реакции), которые могут иногда быть опасными для жизни. На фоне лечения ингибиторами АПФ реакции повышенной чувствительности на яд насекомых (например, пчел, ос) развиваются быстрее и протекают тяжелее. Если необходимо проведение десенсибилизации к яду насекомых, то ингибитор АПФ должен быть временно заменен соответствующим ЛС другого класса. При использовании ингибиторов АПФ были описаны опасные для жизни, быстро развивающиеся анафилактоидные реакции, иногда вплоть до развития шока во время проведения гемодиализа или плазмофильтрации с применением определенных высокопроточных мембран (например, полиакрилнитрильных мембран) (см. также инструкции производителей мембран). Необходимо избегать совместного использования рамиприла и такого рода мембран (например, для срочного гемодиализа или гемофильтрации). В данном случае предпочтительно применение других мембран или исключение приема ингибитора АПФ. Сходные реакции наблюдались при аферезе ЛПНП с применением декстрана сульфата. Поэтому данный метод не следует применять у пациентов, получающих ингибитор АПФ. У пациентов с нарушениями функции печени реакция на лечение препаратами рамиприла может быть или усиленной или ослабленной. Кроме этого, у пациентов с тяжелым циррозом печени с отеками и/или асцитом возможна значительная активация РААС, поэтому при лечении этих пациентов следует соблюдать особую осторожность. Перед хирургическим вмешательством (включая стоматологическое) необходимо предупредить хирурга/анестезиолога о применении ингибитора АПФ. Применение ингибитора АПФ у пациентов, подвергающихся обширному хирургическому вмешательству и/или общей анестезии, может привести к выраженному снижению АД, если используются средства для общей анестезии с гипотензивным действием. Это связано с блокированием образования ангиотензина II на фоне компенсаторного повышения активности ренина. В таком случае следует увеличить объем циркулирующей жидкости. Рекомендуется прекратить прием ингибитора АПФ за 24 часа до хирургического вмешательства. На основании результатов эпидемиологических исследований предполагается, что одновременный прием ингибиторов АПФ и инсулина, а также гипогликемических средств для приема внутрь может приводить к развитию гипогликемии. Наибольший риск развития наблюдается в течение первых недель комбинированной терапии, а также у пациентов с нарушением функции почек. У пациентов с сахарным диабетом требуется регулярный контроль гликемии, особенно во время первого месяца терапии ингибиторами АПФ. Рекомендуется вести тщательное наблюдение за новорожденными, которые подвергались внутриутробному воздействию ингибиторами АПФ, для выявления артериальной гипотензии, олигурии и гиперкалиемии. При олигурии необходимо поддержание АД и почечной перфузии путем введения соответствующих жидкостей и сосудосуживающих средств. У таких новорожденных имеется риск развития олигурии и неврологических расстройств, возможно, из-за снижения почечного и мозгового кровотока вследствие снижения АД, вызываемого ингибиторами АПФ. На фоне терапии ингибиторами АПФ может возникать "сухой" кашель. Кашель длительно сохраняется на фоне приема препаратов этой группы и исчезает после их отмены. При появлении у пациента "сухого" кашля следует помнить о возможном ятрогенном характере этого симптома. У пациентов негроидной расы чаще, чем у представителей других рас, на фоне приема ингибиторов АПФ развивается ангионевротический отек. Рамиприл, как и другие ингибиторы АПФ, возможно оказывает менее выраженное антигипертензивное действие у пациентов негроидной расы по сравнению с представителями других рас. Возможно, это различие обусловлено тем, что у пациентов с АГ негроидной расы чаще отмечается низкая активность ренина. Контроль лабораторных показателей до и во время лечения рамиприлом (до 1 раза в месяц в первые 3-6 мес лечения) включает: Контроль функции почек (определение содержания креатинина в сыворотке) При лечении ингибиторами АПФ в первые недели лечения и в последующем рекомендуется проводить контроль функции почек. Особенно тщательный контроль требуется пациентам с СН, нарушением функции почек, после трансплантации почек, пациентам с реноваскулярными заболеваниями, включая пациентов с гемодинамически значимым односторонним стенозом почечной артерии при наличии двух почек (у таких пациентов даже незначительное повышение уровня сывороточного креатинина может быть показателем снижения функции почек). Контроль содержания электролитов Рекомендуется регулярный контроль содержания калия в сыворотке крови. Особенно тщательный мониторинг содержания калия в сыворотке крови требуется пациентам с нарушениями функции почек, значимыми нарушениями водно-электролитного баланса, ХСН. Контроль гематологических показателей (содержание гемоглобина, количества лейкоцитов, эритроцитов, тромбоцитов, лейкоцитарная формула) Рекомендуется контролировать показатели общего анализа крови для выявления возможной лейкопении. Более регулярный мониторинг рекомендуется в начале лечения и у пациентов с нарушением функции почек, а также у пациентов с заболеваниями соединительной ткани или у пациентов, получающих одновременно другие ЛС, способные изменять картину периферической крови. Контроль количества лейкоцитов необходим для раннего выявления лейкопении, что особенно важно у пациентов с повышенным риском ее развития, а также при первых признаках развития инфекции. При выявлении нейтропении (число нейтрофилов меньше 2000/мкл) требуется прекращение лечения рамиприлом. При появлении симптоматики, обусловленной лейкопенией (например, лихорадки, увеличения лимфатических узлов, тонзиллита), необходим срочный контроль картины периферической крови. В случае появления признаков кровоточивости (мельчайших петехий, красно-коричневых высыпаний на коже и слизистых оболочках) необходим также контроль числа тромбоцитов в периферической крови. Определение активности "печеночных" ферментов, концентрации билирубина в крови При появлении желтухи или значимого повышения активности "печеночных" ферментов лечение рамиприлом следует прекратить и обеспечить врачебное наблюдение за пациентом. Влияние на способность управлять транспортными средствами: В период лечения препаратом рекомендуется воздерживаться от управления транспортными средствами и от занятий другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций (возможно головокружение, особенно в начале лечения, и у пациентов, принимающих диуретические ЛС, снижение концентрации внимания). После первой дозы, а также после значительного повышения дозы препарата не рекомендуется управлять транспортными средствами и работать с техническим оборудованием в течение нескольких часов. Условия хранения и отпуска из аптек Условия хранения:При температуре не выше 25 °С. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Эгипрес® Международное непатентованное название:Амлодипин + Рамиприл. Форма выпуска:капсулы. Состав:Состав на 1 капсулу: Действующие вещества: амлодипина безилат 3,475/6,95/6,95/13,9/13,9 мг (что соответствует амлодипина 2,5/5/5/10/10 мг) и рамиприл 2,5/5/10/5/10 мг. Вспомогательные вещества: кросповидон 10/20/40/40/40 мг, гипромеллоза 0,59/1,18/2,36/2,36/2,36 мг, целлюлоза микрокристаллическая 57,41/114,82/229,64/229,64/229,64 мг, глицерил дибегенат 1,025/2,05/4,1/4,1/4,1 мг. Состав твердой желатиновой капсулы (CONI-SNAP 3), код цвета крышки и основания 37350 (капсулы 2,5 мг+2,5 мг): краситель железа оксид красный (Е172), титана диоксид, желатин. Состав твердой желатиновой капсулы (CONI-SNAP 3), код цвета крышки и основания 51072 (капсулы 5 мг+5 мг): краситель бриллиантовый голубой (Е133), краситель красный очаровательный (Е129), титана диоксид, желатин. Состав твердой желатиновой капсулы (CONI-SNAP 0), код цвета крышки и основания: 51072/37350 (капсулы 5 мг+10 мг): крышка: титана диоксид, краситель бриллиантовый голубой (Е133), краситель красный очаровательный (Е129), желатин: основание: титана диоксид, краситель железа оксид красный (Е172), желатин. Состав твердой желатиновой капсулы (CONI-SNAP 0), код цвета крышки и основания: 33007/37350 (капсулы 10 мг+5 мг): крышка: титана диоксид, краситель азорубин (Е122), индигокармин (Е132), желатин: основание: титана диоксид, краситель железа оксид красный (Е172), желатин. Состав твердой желатиновой капсулы (CONI-SNAP 0), код цвета крышки и основания: 33007 (капсулы 10 мг+10 мг): краситель азорубин (Е122), индигокармин (Е132), титана диоксид, желатин. АТХ: Регистрация: Лекарственное средство ЛП-002402 Фармгруппа: гипотензивное средство комбинированное (ангиотензинпревращающего фермента ингибитор + блокатор "медленных" кальциевых каналов)Дата регистрации: 18.03.2014. Окончание регстрации: . Описание:Капсулы 2,5 мг+2,5 мг: Твердые желатиновые капсулы CONI-SNAP 3, самозакрывающиеся, с основанием и крышкой светло-розового цвета, содержащие смесь гранул и порошков белого или почти белого цвета, без или почти без запаха. Капсулы 5 мг+5 мг: Твердые желатиновые капсулы CONI-SNAP 3, самозакрывающиеся, с основанием и крышкой светло-бордового цвета, содержащие смесь гранул и порошков белого или почти белого цвета, без или почти без запаха. Капсулы 5 мг+10 мг: Твердые желатиновые капсулы CONI-SNAP 0, самозакрывающиеся, с основанием светло-розового цвета и крышкой светло-бордового цвета, содержащие смесь гранул и порошков белого или почти белого цвета, без или почти без запаха. Капсулы 10 мг+5 мг: Твердые желатиновые капсулы CONI-SNAP 0, самозакрывающиеся, с основанием светло-розового цвета и крышкой темно-бордового цвета, содержащие смесь гранул и порошков белого или почти белого цвета, без или почти без запаха. Капсулы 10 мг+10 мг: Твердые желатиновые капсулы CONI-SNAP 0, самозакрывающиеся, с основанием и крышкой темно-бордового цвета, содержащие смесь гранул и порошков белого или почти белого цвета, без или почти без запаха. Упаковка:Капсулы 2,5 мг+2,5 мг, 5 мг+5 мг, 5 мг+10 мг, 10 мг+5 мг, 10 мг+ 10 мг. По 7 или 10 капсул в блистере из комбинированной пленки "cold" (поли- амид/алюминиевая фольга УПВХ)//алюминиевая фольга. 4 или 8 блистеров (по 7 капсул) или 3 или 9 блистеров (по 10 капсул) в картонной пачке вместе с инструкцией по применению. Срок годности:3 года. Не использовать по истечении срока годности, указанного на упаковке. Владелец рег.удостоверения:Эгис Фармацевтический завод ОАО Производитель:EGIS PHARMACEUTICALS, Plc. Представительство:ЭГИС ЗАО фармацевтический завод

Модель:
RUR 0
Показания -Нарушение церебрального кровообращения на фоне атеросклеротического поражения сосудов головного мозга и церебральной сосудистой недостаточности, особенно в пожилом возрасте. -Нарушения периферического кровообращения: синдром "перемежающейся" хромоты, болезнь и синдром Рейно, судороги икроножных мышц, боль в ногах в состоянии покоя, парестезии, акроцианоз. Трофические нарушения (длительно незаживающие язвы, диабетическая ретинопатия). Противопоказания Противопоказания Повышенная индивидуальная чувствительность к препарату, инфаркт миокарда (острая стадия): артериальная гипотензия: геморрагический инсульт (острая стадия): эпилепсия, повышенная судорожная готовность: хроническая сердечная недостаточность II-Ш ст. (III-IV по NYHA - функциональная классификация сердечной недостаточности Нью-Йоркской ассоциации кардиологов): тахиаритмии. Возраст до 18 лет (эффективность и безопасность не установлены. С осторожностью: закрытоугольная глаукома, гиперплазия простаты. Беременность Дузофарм не обладает тератогенным действием, но т.к. специальных исследований его безопасности у беременных женщин не проводилось, рекомендуется назначать препарат только в случаях, когда польза лечения для матери превышает потенциальный риск для плода. Не рекомендуется прием препарата во время кормления грудью. Применение и дозы Внутрь. Таблетки принимаются целиком с количеством жидкости не менее стакана, рекомендуется запивать водой. Дузофарм показан для длительной пероральной терапии. При нарушениях церебрального кровообращения: рекомендуется прием препарата в суточной дозе от 300 мг до 600 мг, разделенной на три приема в разовой дозе 100 мг. При нарушениях периферического кровообращения: рекомендуется прием препарата в суточной дозе от 400 до 600 мг, в разовой дозе 200 мг. Длительность терапии и дозирование определяются врачом в зависимости от клинического состояния пациента. Коррекции дозы при почечпой/печеночной недостаточности не требуется. Побочные эффекты и передозировка Побочные эффекты: При приеме внутрь в дозах от 300 до 600 мг Дузофарм хорошо переносится в целом. Тошнота, рвота, боль в эпигастральной области, кишечные колики, диарея, снижение аппетита, головнаяболь, головокружение, нарушение сна, обратимые повышения активности печеночных ферментов, язвы слизистой оболочки желудка, аллергические реакции. Передозировка: Симптомы: усиление выраженности побочных эффектов, желудочковая аритмия, беспокойство, снижение артериального давления, брадикардия. Лечение: промывание желудка, назначение активированного угля и слабительных препаратов, симптоматическое лечение. Специфического антидота нет. Взаимодействие с другими ЛС: Усиливает гипотензивный эффект антигипертензивных препаратов. В связи с этим рекомендуется более частый контроль артериального давления в начале лечения Дузофармом и антигипертензивными средствами одновременно. Фармакологическое действие и фармакокинетика Нафтидрофурил обладает сосудорасширяющим действием, в результате чего улучшает периферическое и мозговое кровообращение. Вызывает снижение периферического сосудистого сопротивления и увеличивает минутный объем сердца, не оказывая при этом существенного влияния на частоту сердечных сокращений и артериальное давление. Вазодилатирующий эффект нафтидрофурила является результатом его селективного действия на 5НТ2-рецепторы тромбоцитов и гладкомышечного слоя сосудов. В следствии вазодилатации, обусловленной действием нафтидрофурила, отмечается улучшение микроциркуляции в периферических тканях, головном мозге и се тчатке глаза. Оказывает М-холиноблокирующее действие. В условиях ишемии нафтидрофурил вызывает уменьшение анаэробного метаболизма, что приводит к увеличению концентрации адснозиптрифосфата и снижению лактатпируватного коэффициента. В результате повышается устойчивость клеток (в т.ч. мозга) к гипоксии. Препарат улучшает когнитивную функцию мозга, снижает эпизоды головокружения и головной боли, индуцирует улучшение сна. Нафтидрофурил улучшает реологию крови посредством торможения агрегации тромбоцитов и увеличения эластических свойств эритроцитов. Фармакокинетика: Нафтидрофурил почти полностью всасывается при приеме внутрь. Пища практически не оказывает влияния на его всасывание. После приема однократной дозы 100 мг максимальная плазменная концентрация наблюдается через 45-60 минут и составляет 175 мкг/мл. 11одвергается печеночной рециркуляции, что способствует его более длительному нахождению в плазме. Связь с белками крови - 80%. Проникает через гематоэнцефалический барьер. Максимальная концентрация в мозговой ткани наблюдается через 60 минут. Через 24 ч. после приема его концентрация в тканях мозга в 3 раза выше, чем в плазме. Нет данных о проникновении пафтидрофурпла через плаценту и в грудное молоко. Метаболизируется в основном в печени путем гидролиза, который осуществляется плазменными эстеразами. Основными изученными метаболитами являются нафроновая кислота и диэтиламиноэтанол, который обладает стимулирующим действие на цен тральную нервную систему. Период иолувыведения составляет 1-2 часа при приеме однократной дозы 100 мг и 3,5 часа -при приеме 200 мг. Выводится из организма в основном через кишечник и в небольшом количестве почками. Нет данных об изменении скорости его выведения при нарушении функции печени или почек. Возраст не оказывает влияния на фармакокинетические параметры препарата. Особые указания В начале лечения рекомендуется проконтролировать индивидуальную переносимость препарата и проследить возможное гипотензивное действие у соответствующих пациентов. Лекарственный препарат содержит лактозу моногидрат, поэтому является неподходящим для лиц, страдающих лактозной недостаточностью, галактоземией или глюкозо- галактозным синдромом мальабсорбции. Пациентам с целиакией (глютеновой энтеропатией) следует учитывать, что в состав таблетки входит пшеничный крахмал. Влияние на способность управлять транспортными средствами: Дузофарм не оказывает отрицательного влияния на психомоторные реакции и способность водить машину. Условия хранения и отпуска из аптек Условия хранения:В сухом, защищенном от света и недоступном для детей месте при температуре не выше 25°С. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Дузофарм® Международное непатентованное название:Нафтидрофурил. Форма выпуска:таблетки покрытые пленочной оболочкой. Состав:1 таблетка, покрытая пленочной оболочкой, содержит: активное вещество: нафтидрофурила оксалат 50 мг. вспомогательные вещества: лактозы моногидрат 47,50 мг, микрокристаллическая целлюлоза 63,50 мг, пшеничный крахмал 28,00 мг, гликолят натрия крахмал (тип А) 4,80 мг, коповидон 10,00 мг, кросновндон 4.80, кремния диоксид коллоидный 4,00 мг, стеарат магния 7,20 мг, тальк 10,20 мг. состав пленочной оболочки: титана диоксид 1,04 мг, тальк 1,99 мг, макрогол 6000 0,182 мг, метакриловой кислоты и этилакрилата сополимер 0,68 мг, дибутил фталат 0,068 мг, краситель солнечный закат желтый E110. АТХ: Регистрация: ЛСР-002740/09 Фармгруппа: вазодилатирующее средство. Дата регистрации: 07.04.2009. Окончание регстрации: . Описание:Круглые двояковыпуклые таблетки, покрытые пленочной оболочкой, оранжевого цвета. Упаковка:Таблетки, покрытые пленочной оболочкой 50 мг. По 10 таблеток покрытых пленочной оболочкой в блистер из ПВХ /алюминиевой фольги. По 3, 6 или 9 блистеров вместе с инструкцией по применению в картонную пачку. Срок годности:3 года. Не принимать по истечении срока годности, указанного на упаковке! Владелец рег.удостоверения:ЕСКО ФАРМА, ООО Производитель:UNIPHARM, AD. Представительство:ЕСКО ФАРМА, ООО
Модель:
RUR 107
Показания Эссенциальная гипертензия любой степени тяжести. - Реноваскулярная гипертензия. - Сердечная недостаточность любой степени тяжести. У пациентов с наличием клинических проявлений СН препарат Ренитек® также показан для: - повышения выживаемости пациентов: - замедления прогрессирования СН: - снижения частоты госпитализаций по поводу СН. - Профилактика развития клинически выраженной сердечной недостаточности. У пациентов без клинических симптомов СН с дисфункцией левого желудочка препарат Ренитек® показан для: - замедления развития клинических проявлений СН: - снижения частоты госпитализаций по поводу СН. - Профилактика коронарной ишемии у пациентов с дисфункцией левого желудочка. Препарат Ренитек" показан для: - уменьшения частоты развития инфаркта миокарда: снижения частоты госпитализаций по поводу нестабильной стенокардии. Противопоказания Противопоказания - Повышенная чувствительность к любому из компонентов препарата. - Ангионевротический отек в анамнезе, связанный с приемом ингибиторов АПФ, а также наследственный или идиопатический ангионевротический отек. - Одновременное применение с алискиреном или алискиренсодержащими препаратами у пациентов с сахарным диабетом и/или нарушением функции почек (СКФ менее 60 мл/мин/1,73 м 2) (см. раздел "Взаимодействие с другими лекарственными средствами"). - Возраст до 18 лет (эффективность и безопасность не установлены). - Беременность и период грудного вскармливания. - Наследственная непереносимость лактозы, дефицит лактазы, синдром глюкозо-галактозной мальабсорбции. С осторожностью: Двусторонний стеноз почечных артерий или стеноз артерии единственной почки: состояния после трансплантации почки: аортальный или митральный стеноз: гипертрофическая обструктивная кардиомиопатия: ишемическая болезнь сердца или цереброваскулярные заболевания: почечная недостаточность: реноваскулярная гипертензия: угнетение костномозгового кроветворения: системные заболевания соединительной ткани (системная красная волчанка, склеродермия и др.), иммуносупрессивная терапия, лечение с применением аллопуринола или прокаинамида, или комбинация указанных осложняющих факторов: печеночная недостаточность: сахарный диабет: гиперкалиемия: при одновременном применении с калийсберегающими диуретиками, препаратами калия, калийсодержащими заменителями поваренной соли и препаратами лития: при проведении процедуры афереза липопротеинов низкой плотности (ЛПНП-афереза) с использованием декстран сульфата: отягощенный аллергологический анамнез или ангионевротический отек в анамнезе: состояния, сопровождающиеся снижением объема циркулирующей крови (в том числе при терапии диуретиками, соблюдении диеты с ограничением поваренной соли, диализе, диарее или рвоте): во время проведения десенсибилизации аллергеном из яда перепончатокрылых: у пациентов, находящихся на диализе с применением высокопроточных мембран (таких как AN 69 ): у пациентов после больших хирургических вмешательств или при проведении общей анестезии: у пациентов негроидной расы. Беременность Применение препарата Ренитек® во время беременности не рекомендуется. При диагностировании беременности прием препарата Ренитек 8 должен быть немедленно прекращен, если только прием препарата не считается жизненно необходимым для матери. В опубликованных результатах ретроспективного эпидемиологического исследования новорожденных, матери которых принимали ингибиторы АПФ в течение первого триместра беременности, отмечали повышенный риск развития серьезных врожденных пороков развития по сравнению с новорожденными, чьи матери не принимали ингибиторы АПФ в течение первого триместра беременности. Количество случаев врожденных дефектов было низким, и результаты данного исследования не были повторно подтверждены. Ингибиторы АПФ могут вызывать заболевание или гибель плода или новорожденного при применении их беременными во время второго и третьего триместров беременности. Применение ингибиторов АПФ в данные периоды сопровождалось отрицательным воздействием на плод и новорожденного, которое проявлялось в виде артериальной гипотензии, почечной недостаточности, гиперкалиемии и/или гипоплазии костей черепа у новорожденного. Также сообщалось о недоношенности, задержке внутриутробного развития плода и незаращении артериального (Боталлова) протока, однако неясно, были ли эти случаи связаны с действием ингибиторов АПФ. Возможно, развитие олигогидрамниона происходит вследствие снижения функции почек плода. Это осложнение может приводить к контрактуре конечностей, деформации костей черепа, включая его лицевую часть, гипоплазии легких плода. При назначении препарата Ренитек® во время беременности необходимо информировать пациентку относительно потенциального риска для плода. Данные нежелательные эффекты на эмбрион и плод, по-видимому, не являются результатом внутриутробного действия ингибиторов АПФ во время первого триместра беременности. В тех редких случаях, когда применение ингибитора АПФ во время беременности считается необходимым, следует проводить периодические ультразвуковые обследования для оценки индекса амниотической жидкости. В случае выявления в ходе ультразвукового обследования олигогидрамниона необходимо прекратить прием препарата Ренитек®, если только прием препарата не считается жизненно необходимым для матери. Тем не менее, и пациентка, и врач должны знать, что олигогидрамнион развивается при необратимом повреждении плода. Если ингибиторы АПФ применяются во время беременности и наблюдается развитие олигогидрамниона, то в зависимости от недели беременности для оценки функционального состояния плода может быть необходимо проведение стрессового теста, нестрессового теста или определение биофизического профиля плода. Новорожденные, чьи матери принимали препарат Ренитек® во время беременности, должны быть тщательно обследованы в отношении выявления артериальной гипотензии, олигурии и гиперкалиемии. При развитии олигурии особое внимание должно быть направлено на поддержание АД и почечной перфузии. Эналаприл проникает через плацентарный барьер. Он может быть частично удален из кровообращения новорожденного с помощью перитонеального диализа. Теоретически он также может быть удален посредством обменного переливания крови. Эналаприл и эналаприлат выделяются с грудным молоком матери в следовых количествах. В случае необходимости применения препарата в период грудного вскармливания пациентка должна прекратить кормление грудью. Применение и дозы Препарат Ренитек® принимают внутрь, независимо от приема пищи. Эссенциальная гипертензия Начальная доза составляет 10-20 мг в зависимости от степени тяжести АГ и применяется 1 раз в сутки. При мягкой степени АГ рекомендуемая начальная доза составляет 10 мг 1 раз в сутки. При других степенях АГ начальная доза составляет 20 мг 1 раз в сутки. Поддерживающая доза- 1 таблетка 20 мг 1 раз в сутки. Дозировка подбирается индивидуально для каждого пациента, но максимальная доза не должна превышать 40 мг в сутки. Реноваскулярная гипертензия Поскольку у пациентов данной группы АД и почечная функция могут быть особенно чувствительны к ингибированию АПФ, терапию начинают с низкой начальной дозы - 5 мг и менее. Затем доза подбирается в соответствии с потребностями и состоянием пациента. Обычно эффективная доза 20 мг препарата Ренитек® 1 раз в сутки при ежедневном приеме. Следует соблюдать осторожность при применении препарата Ренитек® у пациентов, которые незадолго до этого принимали диуретики (см. ниже Сопутствующее лечение АГ диуретиками). Сопутствующее лечение АГ диуретиками После первого приема препарата Ренитек® может развиться симптоматическая артериальная гипотензия. Такой эффект наиболее вероятен у пациентов, которые принимают диуретики. Препарат рекомендуется применять с осторожностью, так как у данных пациентов может наблюдаться нарушение водно-электролитного баланса. Прием диуретиков следует прекратить за 2-3 дня до начала терапии препаратом Ренитек®. Если это невозможно, то начальную дозу препарата Ренитек® следует снизить (до 5 мг или менее) для определения первичного эффекта препарата на АД. Далее дозировку следует подбирать с учетом потребности и состояния пациента. Дозировка при почечной недостаточности Должен быть увеличен интервал между приемами препарата Ренитек® и/или уменьшена доза. ТАБЛИЦЪ См. разделы "С осторожностью", "Особые указания". * Эналаприл подвергается диализу. Коррекция дозы в дни, когда диализ не проводится, должна осуществляться в зависимости от уровня АД. Сердечная недостаточность/бессимптомная дисфункция левого желудочка Начальная доза препарата Ренитек® у пациентов с клинически выраженной СН или с бессимптомной дисфункцией левого желудочка составляет 2,5 мг. При этом применение препарата должно проводиться под тщательным врачебным контролем для определения первичного эффекта препарата на АД. Препарат Ренитек® может применяться для лечения СН с выраженными клиническими проявлениями обычно совместно с диуретиками и, когда необходимо, с сердечными гликозидами. В случае отсутствия симптоматической артериальной гипотензии (возникшей в результате лечения препаратом Ренитек®) или после ее коррекции дозу препарата следует постепенно повышать до обычной поддерживающей дозы 20 мг, которая применяется либо однократно, либо делится на 2 приема в зависимости от переносимости препарата пациентом. Подбор дозы может проводиться в течение 2-4 недель или в более короткие сроки, если имеются остаточные признаки и симптомы СН. Такой терапевтический режим эффективно снижает показатели смертности пациентов с клинически выраженной СН. Как до, так и после начала лечения препаратом Ренитек® следует проводить регулярный контроль АД и функции почек (см. раздел "Особые указания"), поскольку сообщалось о развитии в результате приема препарата артериальной гипотензии с последующим (более редко) возникновением острой почечной недостаточности. У пациентов, принимающих диуретики, доза диуретиков по возможности должна быть снижена до начала лечения препаратом Ренитек®. Развитие артериальной гипотензии после приема первой дозы препарата Ренитек® не означает, что артериальная гипотензия повторно разовьется при длительном лечении, и не указывает на необходимость прекращения приема препарата. При лечении препаратом Ренитек® следует также контролировать содержание калия в сыворотке крови (см. раздел "Взаимодействие с другими лекарственными средствами"). Побочные эффекты и передозировка Побочные эффекты: В целом препарат Ренитек® хорошо переносится. В клинических исследованиях суммарная частота нежелательных явлений при применении препарата Ренитек® не превышала таковую при приеме плацебо. В большинстве случаев нежелательные явления были легкими, преходящими и не требовали отмены терапии. При применении препарата Ренитек® наблюдались следующие нежелательные явления (очень частые: >: или = 10%, частые: >: или = 1% и <: 10%, нечастые: >: или = 0,1% и <: 1%, редкие: >: или = 0,01% и <: 0,1%, очень редкие: <: 0,01%, частота неизвестна: невозможно оценить частоту на основании доступных данных): Нарушения со стороны крови и лимфатической системы Нечастые: анемия (включая апластическую и гемолитическую). Редкие: нейтропения, снижение гемоглобина, снижение гематокрита, тромбоцитопения, агранулоцитоз, подавление функции костного мозга, панцитопения, лимфаденопатия, аутоиммунные заболевания. Нарушения со стороны эндокринной системы Частота не установлена: синдром неадекватной секреции антидиуретического гормона. Нарушения со стороны обмена веществ и питания Нечастые: гипогликемия (см. раздел "Особые указания"). Нарушения со стороны нервной системы и нарушения психики Частые: головная боль, депрессия. Нечастые: спутанность сознания, сонливость, бессонница, повышенная нервозность, парестезия, системное головокружение. Редкие: необычные сновидения, нарушения сна. Нарушения со стороны органа зрения Очень частые: нечеткость зрения. Нарушения со стороны сердца и сосудов Очень частые: головокружение. Частые: выраженное снижение АД, обморок, боль в груди, нарушение ритма, стенокардия, тахикардия. Нечастые: ортостатическая гипотензия, ощущение сердцебиения, инфаркт миокарда или инсульт, возможно, вторичные по отношению к выраженной артериальной гипотензии у пациентов, относящихся к группе высокого риска (см. раздел "Особые указания"). Редкие: синдром Рейно. Нарушения со стороны дыхательной системы, органов грудной клетки и средостения Очень частые: кашель. Частые: одышка. Нечастые: ринорея, боль в горле, охриплость голоса, бронхоспазм/бронхиальная астма. Редкие: легочные инфильтраты, риниты, аллергический альвеолит/эозинофильная пневмония. Нарушения со стороны пищеварительной системы Очень частые: тошнота. Частые: диарея, боли в области живота, нарушение вкуса. Нечастые: кишечная непроходимость, панкреатит, рвота, диспепсия, запор, анорексия, раздражение желудка, сухость слизистой оболочки полости рта, язва желудка и двенадцатиперстной кишки. Редкие: стоматит/афтозные язвы, глоссит. Очень редкие: интестинальный отек. Нарушения со стороны печени и желчевыводящих путей Редкие: печеночная недостаточность, гепатит (гепатоцеллюлярный или холестатический), гепатит (включая некроз), холестаз (включая желтуху). Нарушения со стороны кожи и подкожных тканей Частые: кожная сыпь, реакции гиперчувствительносги/ангионевротический отек: ангионевротический отек лица, конечностей, губ, языка, голосовых складок и/или гортани (см. раздел "Особые указания"). Нечастые: повышенное потоотделение, кожный зуд, крапивница, алопеция. Редкие: многоформная эритема, синдром Стивенса-Джонсона, эксфолиативный дерматит, токсический эпидермальный некролиз, пемфигус, эритродермия. Сообщалось о развитии симптомокомплекса, который может включать все или некоторые из следующих симптомов: лихорадку, серозит, васкулит, миалгию/миозит, артралгию/артрит, положительный тест на антинуклеарные антитела, увеличение скорости оседания эритроцитов (СОЭ), эозинофилию и лейкоцитоз. Могут также возникать кожная сыпь, фотосенсибилизация и другие кожные реакции. Нарушения со стороны почек и мочевыводящих путей Нечастые: нарушения функции почек, почечная недостаточность, протеинурия. Редкие: олигурия. Нарушения со стороны половых органов и молочной железы Нечастые: эректильная дисфункция. Редкие: гинекомастия. Общие расстройства Очень частые: астения. Частые: повышенная утомляемость. Нечастые: мышечные судороги, "приливы" крови к коже лица, шум в ушах, чувство дискомфорта, лихорадка. Лабораторные и инструментальные данные Частые: гиперкалиемия, увеличение концентрации сывороточного креатинина. Нечастые: повышение концентрации мочевины в крови, гипонатриемия. Редкие: повышение активности "печеночных" трансаминаз, увеличение концентрации билирубина в сыворотке крови. Частота случаев была сравнима с частотой, наблюдавшейся в клинических исследованиях при приеме плацебо или другого препарата сравнения. Перечисленные ниже нежелательные явления выявлены в ходе пострегистрационного наблюдения, однако причинно-следственной связи с приемом препарата Ренитек® не установлено: инфекция мочевыводящих путей, инфекция верхних дыхательных путей, бронхит, остановка сердца, фибрилляция предсердий, опоясывающий герпес, мелена, атаксия, тромбоэмболия ветвей легочной артерии и инфаркт легкого, гемолитическая анемия, включая случаи гемолиза у пациентов с дефицитом глюкозо-6-фосфатдегидрогеназы. Передозировка: Сведения о передозировке ограничены. Наиболее характерные симптомы передозировки: выраженное снижение АД, начинающееся приблизительно через 6 ч после приема препарата одновременно с блокадой РААС, и ступор. Концентрации эналаприлата в сыворотке крови, превышающие в 100 и 200 раз концентрации, наблюдающиеся при применении терапевтических доз, возникали после приема соответственно 300 и 440 мг эналаприла. Рекомендуемое лечение передозировки: внутривенная инфузия 0,9% раствора натрия хлорида. Если препарат был принят недавно- провокация рвоты. Эналаприлат может быть удален из системного кровообращения с помощью гемодиализа (см. раздел "Особые указания, Пациенты на гемодиализе"). Взаимодействие с другими ЛС: Другие гипотензивные средства Аддитивный эффект может наблюдаться при одновременном применении препарата Ренитек® и другой гипотензивной терапии. При применении препарата Ренитек® одновременно с другими гипотензивными средствами, особенно с диуретиками, может наблюдаться усиление антигипертензивного эффекта. Одновременное применение препарата Ренитек® с бета-адреноблокаторами, метилдопой или блокаторами "медленных" кальциевых каналов повышало выраженность антигипертензивного эффекта. Одновременное применение препарата Ренитек® с альфа, бета-адреноблокаторами и ганглиоблокаторами должно проводиться под тщательным врачебным контролем. Одновременное применение препарата Ренитек® с нитроглицерином, другими нитропрепаратами или другими вазодилататорами усиливает антигипертензивный эффект. Калий сыворотки крови В клинических исследованиях содержание калия в сыворотке крови обычно оставалось в пределах нормы. У пациентов с АГ, принимавших препарат Ренитек® в монотерапии более 48 недель, наблюдалось увеличение содержания калия в сыворотке крови в среднем на 0,2 ммоль/л. При одновременном применении препарата Ренитек® с диуретиками, вызывающими потерю ионов калия (тиазиды или "петлевые" диуретики), гипокалиемия, вызванная действием диуретиков, как правило, ослабляется благодаря эффекту эналаприла. Факторами риска для развития гиперкалиемии являются почечная недостаточность, сахарный диабет, одновременное применение калийсберегающих диуретиков (например, спиронолактона, эплеренона, триамтерена или амилорида), а также калийсодержащих добавок и солей. Применение калиевых добавок, калийсберегающих диуретиков или калийсодержащих солей, особенно у пациентов с нарушением функции почек, может привести к значительному возрастанию содержания калия в сыворотке крови. При необходимости одновременного применения перечисленных выше калийсодержащих или повышающих содержание калия препаратов следует соблюдать осторожность и регулярно контролировать содержание калия в сыворотке крови. Гипогликемические средства Эпидемиологические исследования показали, что одновременное применение ингибиторов АПФ и гипогликемических средств (инсулина, гипогликемических средств для приема внутрь) может усилить гипогликемический эффект последних с риском развития гипогликемии. Данный феномен, как правило, наиболее часто наблюдался в течение первых недель комбинированной терапии, а также у пациентов с нарушением функции почек. У пациентов с сахарным диабетом, принимающих гипогликемические средства для приема внутрь или инсулин, следует регулярно контролировать концентрацию глюкозы крови, особенно в течение первого месяца одновременного применения с ингибиторами АПФ. Препараты лития Как и другие лекарственные средства, влияющие на выведение натрия, ингибиторы АПФ могут снижать выведение лития почками, поэтому при одновременном применении препаратов лития и ингибиторов АПФ необходимо регулярно мониторировать концентрацию лития в сыворотке крови. Трициклические антидепрессанты/нейролептики/средства для общей анестезии/ наркотические средства Одновременное применение некоторых анестезирующих лекарственных средств, трициклических антидепрессантов и нейролептики с ингибиторами АПФ может привести к дальнейшему снижению АД (см. раздел "Особые указания"). Этанол Этанол усиливает антигипертензивное действие ингибиторов АПФ. Ацетилсалициловая кислота, тромболитики и бета-адреноблокаторы Эналаприл можно применять одновременно с ацетилсалициловой кислотой (в качестве антиагрегантного средства), тромболитиками и бета-адреноблокаторами. Симпатомиметики Симпатомиметики могут снижать антигипертензивный эффект ингибиторов АПФ. Нестероидные противовоспалительные препараты (НПВП) НПВП, в том числе селективные ингибиторы циклооксигеназы-2 (ЦОГ-2), могут снижать эффект диуретиков и других гипотензивных средств. Вследствие этого антигипертензивный эффект антагонистов рецепторов ангиотензина II (АРА II) или ингибиторов АПФ может быть ослаблен при одновременном применении с НПВП, в том числе с селективными ингибиторами ЦОГ-2. У некоторых пациентов с нарушенной функцией почек (например, у пожилых пациентов или пациентов с обезвоживанием, в том числе принимающих диуретики), получающих терапию НПВП, в том числе селективными ингибиторами ЦОГ-2, одновременное применение АРА II или ингибиторов АПФ может вызвать дальнейшее ухудшение функции почек, включая развитие острой почечной недостаточности. Данные эффекты обычно обратимы, поэтому одновременное применение данных лекарственных средств должно проводиться с осторожностью у пациентов с нарушенной функцией почек. Двойная блокада ренин-ангиотензнн-альдостероновой системы Двойная блокада РААС с применением АРА II, ингибиторов АПФ или алискирена (ингибитор ренина) ассоциирована с повышенным риском развития артериальной гипотензии, обморока, гиперкалиемии и нарушений функции почек (в том числе острой почечной недостаточности) по сравнению с монотерапией. Необходим регулярный контроль АД, функции почек и содержания электролитов в крови у пациентов, принимающих одновременно препарат Ренитек® и другие лекарственные средства, влияющие на РААС. Препарат Ренитек® не должен применяться одновременно с алискиреном или алискиренсодержащими препаратами у пациентов с сахарным диабетом и/или с нарушением функции почек (СКФ менее 60 мл/мин/1,73 м 2). Препараты золота Симптомокомплекс (нитратоподобные реакции), включающий "прилив" крови к коже лица, тошноту, рвоту и артериальную гипотензию, наблюдался в редких случаях при одновременном применении препаратов золота для парентерального введения (натрия ауротиомалат) и ингибиторов АПФ. включая эналаприл. Другие лекарственные средства Не наблюдалось клинически значимого фармакокинетического лекарственного взаимодействия между препаратом Ренитек® и следующими лекарственными средствами: гидрохлоротиазидом, фуросемидом, дигоксином, тимололом, метилдопой, варфарином, индометацином, сулиндаком и циметидином. При одновременном применении препарата Ренитек® и пропранолола снижается концентрация эналаприлата в сыворотке крови, но данный эффект не является клинически значимым. Фармакологическое действие и фармакокинетика Препарат Ренитек® (эналаприл) относится к лекарственным средствам, влияющим на ренин-ангиотензин-альдостероновую систему (РААС)- ингибиторам АПФ. Препарат Ренитек® применяется для лечения эссенциальной гипертензии (первичной артериальной гипертензии (АГ)) любой степени тяжести и реноваскулярной гипертензии как в монотерапии, так и в комбинации с другими гипотензивными средствами, в частности с диуретиками. Также препарат Ренитек® применяется для лечения или предупреждения развития сердечной недостаточности (СН). Препарат Ренитек® (эналаприл) является производным двух аминокислот, L-аланина и L-пролина. После приема внутрь эналаприл быстро всасывается и гидролизуется в эналаприлат, который является высокоспецифичным и длительно действующим ингибитором АПФ, не содержащим сульфгидрильную группу.АПФ (пептидил-дипептидаза А) катализирует превращение ангиотензина I в прессорный пептид ангиотензин II. После всасывания эналаприл гидролизуется до эналаприлата, который ингибирует АПФ. Ингибирование АПФ приводит к снижению концентрации ангиотензина II в плазме крови, что влечет за собой увеличение активности ренина плазмы крови (вследствие устранения отрицательной обратной связи в ответ на высвобождение ренина) и уменьшение секреции альдостерона.АПФ идентичен ферменту кининаза II, поэтому эналаприл также может блокировать разрушение брадикинина- пептида, обладающего выраженным вазодилатирующим действием. Значение этого эффекта в терапевтическом действии эналаприла требует уточнения. Несмотря на то, что основным механизмом, при помощи которого эналаприл снижает артериальное давление (АД), считается подавление активности РААС, играющей важную роль в регулировании АД, эналаприл проявляет антигипертензивное действие даже у пациентов с АГ и со сниженной активностью ренина плазмы крови. Применение эналаприла пациентами с АГ приводит к снижению АД как в положении "стоя", так и в положении "лежа" без значимого увеличения частоты сердечных сокращений (ЧСС). Симптоматическая постуральная гипотензия развивается нечасто. У некоторых пациентов достижение оптимального снижения АД может потребовать нескольких недель терапии. Прерывание терапии эналаприлом не вызывает резкого подъема АД. Эффективное ингибирование активности АПФ обычно развивается через 2-4 ч после однократного приема дозы эналаприла внутрь. Антигипертензивное действие развивается в течение I ч, максимальное снижение АД наблюдается через 4-6 ч после приема препарата. Продолжительность действия зависит от дозы. Однако при применении рекомендованных доз антигипертензивное действие и гемодинамические эффекты сохраняются в течение 24 ч. Гипотензивная терапия эналаприлом ведет к значительной регрессии гипертрофии левого желудочка и сохранению его систолической функции.В клинических исследованиях гемодинамики у пациентов с эссенциальной гипертензией снижение АД сопровождалось снижением общего периферического сосудистого сопротивления, увеличением сердечного выброса и отсутствием изменений или незначительными изменениями ЧСС. После приема эналаприла наблюдалось увеличение почечного кровотока. При этом скорость клубочковой фильтрации (СКФ) не менялась, не наблюдались признаки задержки натрия или жидкости. Однако у пациентов с исходно сниженной клубочковой фильтрацией ее скорость обычно увеличивалась. Длительное применение эналаприла у пациентов с эссенциальной гипертензией и почечной недостаточностью может привести к улучшению функции почек, что подтверждается увеличением СКФ.В коротких клинических исследованиях у пациентов с почечной недостаточностью и с сахарным диабетом или без наблюдалось снижение альбуминурии, выведения почками IgG. а также снижение общего белка в моче после приема эналаприла. При одновременном применении эналаприла и тиазидных диуретиков наблюдается более выраженное антигипертензивное действие. Эналаприл уменьшает или предупреждает развитие гипокалиемии, вызванной приемом тиазидов. Терапия эналаприлом обычно не связана с нежелательным влиянием на концентрацию мочевой кислоты в плазме крови. Терапия эналаприлом сопровождается благоприятным действием на соотношение фракций липопротеинов в плазме крови и отсутствием влияния или благоприятным действием на концентрацию общего холестерина.У пациентов с СН на фоне терапии сердечными гликозидами и диуретиками прием эналаприла вызывал снижение общего периферического сопротивления и АД. Сердечный выброс увеличивался, в то время как ЧСС (обычно повышенная у пациентов с СН) снижалась. Давление заклинивания в легочных капиллярах также снижалось. Толерантность к физической нагрузке и степень тяжести СН, оцененные по критериям Нью-Йоркской кардиологической ассоциации (NYHA), улучшались. Данные эффекты наблюдались при длительной терапии.У пациентов с легкой и умеренной степенью тяжести СН эналаприл замедлял прогрессирование дилатации сердца и СН, что подтверждалось снижением конечнодиастолического и систолического объемов левого желудочка и улучшением фракции выброса левого желудочка. Клинические данные показали, что эналаприл уменьшает частоту желудочковых аритмий у пациентов с СН, хотя основные механизмы и клиническое значение данного эффекта не известны. Фармакокинетика: Всасывание После приема внутрь эналаприл быстро всасывается в желудочно-кишечном тракте. Максимальная концентрация эналаприла в сыворотке крови достигается в течение 1 ч после приема внутрь. Степень всасывания эналаприла при приеме внутрь составляет приблизительно 60%. Прием пищи не оказывает влияния на всасывание эналаприла. После всасывания эналаприл быстро гидролизуется с образованием активного метаболита эналаприлата- мощного ингибитора АПФ. Максимальная концентрация эналаприлата в сыворотке крови наблюдается приблизительно через 4 ч после приема дозы эналаприла внутрь. Продолжительность всасывания и гидролиза эналаприла сходна для различных рекомендованных терапевтических доз. У здоровых добровольцев с нормальной функцией почек равновесная концентрация эналаприлата в сыворотке крови достигается к 4 дню с начала приема эналаприла. Распределение В диапазоне терапевтических доз связывание эналаприлата с белками плазмы крови не превышает 60%. Метаболизм Нет данных о других значимых путях метаболизма эналаприла, кроме гидролиза до эналаприлата. Выведение Выведение эналаприла осуществляется преимущественно через почки. Основными метаболитами, определяемыми в моче, являются эналаприлат, составляющий приблизительно 40% дозы, и неизмененный эналаприл (приблизительно 20%). Кривая концентрации эналаприлата в плазме крови имеет длительную конечную фазу, по- видимому, обусловленную его связыванием с АПФ. Период полувыведения эналаприлата при курсовом применении препарата внутрь составляет 11 ч. Фармакокинетика у особых групп пациентов Пациенты с нарушенной функцией почек Площадь под кривой "концентрация-время" (AUC) эналаприла и эналаприлата увеличивается у пациентов с почечной недостаточностью. У пациентов с легкой и умеренной степенью тяжести почечной недостаточности (клиренс креатинина (КК) 40- 60 мл/мин) после приема эналаприла в дозе 5 мг 1 раз в сутки равновесное значение AUC эналаприлата было приблизительно в 2 раза выше, чем у пациентов с неизмененной функцией почек. У пациентов с тяжелой почечной недостаточностью (КК не более 30 мл/мин) значение AUC увеличивалось приблизительно в 8 раз. Эффективное время полувыведения эналаприлата после многократного применения эналаприла у пациентов с тяжелой степенью почечной недостаточности увеличивалось, и наступление равновесного состояния концентрации эналаприлата задерживалось (см. раздел "Способ применения и дозы"). Эналаприлат может быть выведен из общего кровотока с помощью процедуры гемодиализа. Клиренс при гемодиализе составляет 62 мл/мин. Лактация После однократного применения внутрь эналаприла в дозе 20 мг у пациенток в послеродовом периоде средняя максимальная концентрация эналаприла в грудном молоке составила 1,7 мкг/л (от 0,54 до 5,9 мкг/л) через 4-6 ч после приема. Средняя максимальная концентрация эналаприлата составила 1,7 мкг/л (от 1,2 до 2,3 мкг/л) и наблюдалась в различное время в течение 24 ч после приема. С учетом данных о максимальных концентрациях в грудном молоке оценочное максимальное потребление эналаприла ребенком, находящимся на полном грудном вскармливании, составляет 0,16% от дозы, рассчитанной с учетом массы тела матери. У женщины, которая принимала эналаприл внутрь в дозе 10 мг 1 раз в сутки в течение 1 I месяцев, максимальные концентрации эналаприла в грудном молоке составили 2 мкг/л через 4 ч после приема, максимальные концентрации эналаприлата- 0.75 мкг/л приблизительно через 9 ч после приема. Средняя концентрация в грудном молоке в течение 24 ч после приема эналаприла составила 1,44 мкг/л и эналаприлата - 0,63 мкг/л. У одной женщины, которая приняла эналаприл в дозе 5 мг однократно, и у двух женщин, которые приняли эналаприл в дозе 10 мг однократно, концентрация эналаприлата в грудном молоке была ниже определяемого уровня (менее 0,2 мкг/л) через 4 ч после приема. Концентрация эналаприла у них не определялась. Особые указания Симптоматическая артериальная гипотензия Симптоматическая артериальная гипотензия редко наблюдается у пациентов с неосложненной АГ. У пациентов с АГ, принимающих препарат Ренитек®, артериальная гипотензия развивается чаще на фоне обезвоживания, возникающего, например, в результате терапии диуретиками, ограничения потребления поваренной соли, у пациентов, находящихся на диализе, а также у пациентов с диареей или рвотой (см. разделы "Побочное действие": "Взаимодействие с другими лекарственными средствами"). Симптоматическая артериальная гипотензия наблюдалась и у пациентов с СН с или без почечной недостаточности. Артериальная гипотензия развивается чаще у пациентов с более тяжелой степенью СН с гипонатриемией или нарушениями функции почек, у которых применяются более высокие дозы "петлевых" диуретиков. У данных пациентов лечение препаратом Ренитек® следует начинать под врачебным контролем, который должен быть особенно тщательным при изменении дозы препарата Ренитек® и/или диуретика. Аналогичным образом следует наблюдать за пациентами с ишемической болезнью сердца или с цереброваскулярными заболеваниями, у которых чрезмерное снижение АД может привести к развитию инфаркта миокарда или инсульта. При развитии артериальной гипотензии пациента следует уложить и в случае необходимости ввести 0,9% раствор натрия хлорида. Транзиторная артериальная гипотензия при приеме препарата Ренитек® не является противопоказанием к дальнейшему применению и увеличению дозы препарата, которое может быть продолжено после восполнения объема жидкости и н



